Ingredientes activos: Flurbiprofeno
GARGANTA CONGELADA 0,25% Enjuague bucal
GARGANTA CONGELADA 0,25% Spray de mucosa oral
¿Por qué se usa la garganta Froben? ¿Para qué sirve?
QUÉ ES
Froben Gola es un fármaco antiinflamatorio no esteroideo para uso orofaríngeo.
POR QUÉ SE UTILIZA
Froben Gola se utiliza para el tratamiento sintomático de estados irritativos-inflamatorios también asociados con dolor orofaríngeo (por ejemplo, gingivitis, estomatitis, faringitis), también como consecuencia de la terapia dental conservadora o extractiva.
Contraindicaciones Cuando no se debe utilizar Froben Threat
Hipersensibilidad al principio activo oa alguno de los excipientes.
Hipersensibilidad a la aspirina u otros AINE.
No lo use en pacientes que tengan úlcera péptica o la hayan tenido en el pasado.
No lo use durante el tercer trimestre del embarazo.
Precauciones de uso Lo que necesita saber antes de tomar Froben garganta
A las dosis recomendadas, la posible ingestión de GARGANTA CONGELADA no causa ningún daño al paciente ya que estas dosis son muy inferiores a las de la dosis única del producto por vía sistémica.
Dada la falta de gas propulsor en la formulación de FROBEN THROAT 0.25% Spray para mucosa oral, al utilizar el producto por primera vez, presionar el dosificador varias veces hasta lograr una nebulización regular.
El uso, especialmente si es prolongado, del producto puede dar lugar a fenómenos de sensibilización o irritación local, en tales casos es necesario interrumpir el tratamiento y consultar al médico para establecer, si es necesario, una terapia adecuada.
Interacciones ¿Qué medicamentos o alimentos pueden modificar el efecto de Froben en la garganta?
Informe a su médico o farmacéutico si ha tomado recientemente otros medicamentos, incluso sin receta.
A las dosis recomendadas, no se han notificado interacciones con otros medicamentos u otros tipos.
Advertencias Es importante saber que:
GARGANTA CONGELADA no debe utilizarse para tratamientos prolongados. Después de breves períodos de tratamiento sin resultados apreciables, consulte a su médico.
Cuando se puede usar solo después de consultar a su médico
Los pacientes que tienen una úlcera péptica o que la han tenido en el pasado deben consultar a su médico antes de tomar Froben Gola.
Qué hacer durante el embarazo y la lactancia.
Consulte a su médico o farmacéutico antes de tomar cualquier medicamento. Durante el primer y segundo trimestre del embarazo, no se debe administrar flurbiprofeno a menos que sea estrictamente necesario. No se recomienda la administración de flurbiprofeno en madres lactantes.
Efectos sobre la capacidad para conducir y utilizar máquinas.
GARGANTA CONGELADA no afecta la capacidad para conducir o utilizar máquinas.
Advertencia de dopaje
Tanto el enjuague bucal como el aerosol para la mucosa oral contienen alcohol etílico.
Para quienes practican deporte, el uso de medicamentos que contienen alcohol etílico puede determinar una prueba antidopaje positiva en relación con los límites de concentración de alcohol indicados por algunas federaciones deportivas.
Notas de educación sanitaria
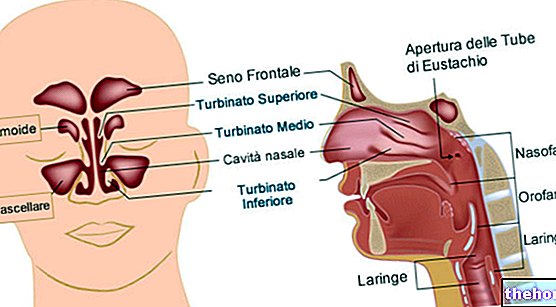
En condiciones ambientales favorables (descenso o cambios bruscos de temperatura, aumento de la tasa de humedad, etc.), el tracto respiratorio superior puede ser el lugar de injerto de gérmenes patógenos que provocan inflamación.
Los síntomas característicos de la inflamación del tracto respiratorio superior (boca, nariz, garganta) incluyen dolor de garganta, sensación de ardor, dificultad para tragar y pueden controlarse parcialmente evitando la exposición a factores irritantes adicionales como humo, smog, aire seco, lugares concurridos. etc.
La inflamación también puede estar presente en las encías, lo que podría ser un signo de problemas dentales en la fase inicial: en este caso, una revisión al dentista podría ser útil para evitar un desarrollo desagradable del trastorno.
Además, como resultado de terapias dentales conservadoras, extracciones dentales, pequeñas cirugías dentales, las encías y la cavidad bucal pueden ser el lugar de enrojecimiento, inflamación y dolor.
Posología y forma de empleo Modo de empleo Froben garganta: Posología
CUÁNTO
Advertencia: no exceda las dosis indicadas.
- Enjuague bucal: La dosis recomendada es de dos o tres enjuagues o gárgaras al día con 10ml de enjuague bucal.
- Spray bucal: la dosis recomendada es de 2 pulverizaciones 3 veces al día.
CUANDO Y POR CUANTO TIEMPO
El medicamento se puede utilizar en cualquier momento del día.
Advertencia: utilícelo solo durante períodos cortos de tratamiento. Consulte a su médico si el trastorno se produce de forma repetida o si nota algún cambio reciente en sus características.
IGUAL QUE
Enjuague bucal:
el producto se puede utilizar en forma pura (10 ml), o alternativamente se puede diluir en agua.
Spray de mucosa oral
Dirija los aerosoles directamente sobre la parte afectada.
ESTRUCIONES POR USAR GARGANTA CONGELADA 0.25% Spray mucoso oral
Gire la boquilla hacia la derecha o hacia la izquierda, sin alterar el dispensador.
Presione el dispensador.
Sobredosis Qué hacer si ha tomado demasiado Froben para la garganta
Síntomas
Los síntomas de una sobredosis pueden incluir náuseas, vómitos e irritación gastrointestinal.
Tratamiento
El tratamiento debe incluir lavado gástrico y, si es necesario, corrección del cuadro de electrolitos séricos.
No existe un antídoto específico para el flurbiprofeno.
En caso de ingestión / ingesta accidental de una dosis excesiva de GARGANTA CONGELADA, notifique a su médico inmediatamente o acuda al hospital más cercano.
SI TIENE ALGUNA DUDA SOBRE EL USO DE GARGANTA CONGELADA, CONTACTE A SU MÉDICO O FARMACÉUTICO
Efectos secundarios ¿Cuáles son los efectos secundarios de la garganta Froben?
Como todos los medicamentos, GARGANTA CONGELADA puede producir efectos adversos, aunque no todas las personas los sufran.
A las dosis recomendadas no se informan efectos indeseables.
Se han notificado las siguientes reacciones adversas, particularmente después de la administración de formulaciones para uso sistémico.
Trastornos del sistema sanguíneo y linfático.
Trombocitopenia, anemia aplásica y agranulocitosis
Trastornos del sistema inmunológico.
Anafilaxia, angioedema, reacción alérgica.
Trastornos del sistema nervioso.
Mareos, accidentes cerebrovasculares, alteraciones visuales, neuritis óptica, migraña, parestesia, depresión, confusión, alucinaciones, vértigo, malestar general, fatiga y somnolencia.
Perturbaciones acústicas y laberínticas
Tinnitus
Trastornos respiratorios, torácicos y mediastínicos
Reactividad del tracto respiratorio (asma, broncoespasmo y disnea)
Desórdenes gastrointestinales
Los eventos adversos observados con mayor frecuencia son de naturaleza gastrointestinal. Se han notificado náuseas, vómitos, diarrea, flatulencia, estreñimiento, dispepsia, dolor abdominal, melena, hematemesis, estomatitis ulcerosa, hemorragia gastrointestinal y exacerbación de colitis y enfermedad de Crohn tras la administración de flurbiprofeno. Se observaron con menor frecuencia gastritis, úlcera péptica, perforación y hemorragia ulcerosa. Muy raramente se han notificado casos de pancreatitis.
Trastornos de la piel y del tejido subcutáneo
Trastornos de la piel que incluyen erupción, prurito, urticaria, púrpura, angioedema y muy raramente dermatosis ampollosa (incluido el síndrome de Stevens-Johnson, necrólisis epidérmica tóxica y eritema multiforme).
Trastornos de los riñones y del sistema urinario.
Nefrotoxicidad en diversas formas, incluida la nefritis intersticial y el síndrome nefrótico.Al igual que con otros AINE, se han notificado casos raros de insuficiencia renal.
El cumplimiento de las instrucciones contenidas en el prospecto reduce el riesgo de reacciones adversas.
Notificación de efectos secundarios
Si experimenta efectos adversos, consulte a su médico o farmacéutico, incluidos los posibles efectos adversos que no aparecen en este prospecto. Los efectos indeseables también pueden notificarse directamente a través del sistema nacional de notificación en "https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse". Al informar los efectos secundarios, puede ayudar a proporcionar más información sobre la seguridad de este medicamento ".
Caducidad y retención
Caducidad: consulte la fecha de caducidad indicada en el paquete. La fecha de caducidad indicada se refiere al producto en envase intacto, correctamente almacenado. Advertencia: no use el medicamento después de la fecha de caducidad indicada en el paquete.
Periodo de validez después de la primera apertura: 1 año.
Enjuague bucal: este medicamento no requiere condiciones especiales de conservación.
Aerosol bucal: este medicamento no requiere ninguna temperatura de almacenamiento particular; mantenga el frasco en el embalaje exterior para proteger el medicamento de la luz.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que no necesita, ya que esto ayudará a proteger el medio ambiente.
MANTENGA EL MEDICAMENTO FUERA DE LA VISTA Y DEL ALCANCE DE LOS NIÑOS
Es importante tener siempre disponible la información sobre el medicamento, así que conserve tanto la caja como el prospecto.
COMPOSICIÓN
GARGANTA CONGELADA 0,25% enjuague bucal
100 ml de solución contienen:
Principio activo: Flurbiprofeno 0,25 g.
Excipientes: agua purificada, alcohol, azul patente VE 131, glicerol, esencia de menta, aceite de ricino hidrogenado de 40 polioxietileno, bicarbonato de potasio, sacarinato de sodio, sorbitol.
GARGANTA CONGELADA 0,25% spray para mucosa bucal
100 ml de solución contienen
El principio activo es flurbiprofeno 0,25 g.
Excipientes: agua purificada, alcohol, azul patente VE 131, glicerol, esencia de menta, aceite de ricino hidrogenado de polioxietileno 40, bicarbonato de potasio, sacarinato de sodio, sorbitol.
CÓMO SE VE
Enjuague bucal al 0,25% - 1 frasco de 160 ml Spray bucal al 0,25% - 1 frasco de 15 ml
Prospecto fuente: AIFA (Agencia Italiana de Medicamentos). Contenido publicado en enero de 2016. Es posible que la información presente no esté actualizada.
Para tener acceso a la versión más actualizada, es recomendable acceder al sitio web de la AIFA (Agencia Italiana de Medicamentos). Descargo de responsabilidad e información útil.
01.0 NOMBRE DEL MEDICAMENTO
GARGANTA CONGELADA 0.25%
02.0 COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
• GARGANTA CONGELADA 0,25% Enjuague bucal
100 ml de solución contienen:
Principio activo:
Flurbiprofeno 0,25 g
• GARGANTA CONGELADA 0,25% Spray para mucosa bucal
100 ml de solución contienen:
Principio activo:
Flurbiprofeno 0,25 g
Para consultar la lista completa de excipientes, ver sección 6.1.
03.0 FORMA FARMACÉUTICA
Enjuague bucal
Spray de mucosa oral
04.0 INFORMACIÓN CLÍNICA
04.1 Indicaciones terapéuticas
Tratamiento sintomático de estados irritativos-inflamatorios también asociados con dolor orofaríngeo (por ejemplo, gingivitis, estomatitis, faringitis), también como consecuencia de la terapia dental conservadora o extractiva.
04.2 Posología y forma de administración
Las reacciones adversas pueden minimizarse utilizando la dosis eficaz más baja durante el tratamiento más breve posible necesario para controlar los síntomas (ver sección 4.4).
ENJUAGUE BUCAL
La dosis recomendada es de dos o tres enjuagues o gárgaras al día con 10ml de enjuague bucal. Se puede diluir en agua.
SPRAY PARA MUCOSA ORAL
La dosis recomendada es de 2 pulverizaciones 3 veces al día dirigidas directamente a la zona afectada.
04.3 Contraindicaciones
El flurbiprofeno está contraindicado en pacientes con hipersensibilidad conocida (asma, urticaria o tipo alérgico) al flurbiprofeno oa cualquiera de los excipientes, así como a la aspirina u otros AINE.
El flurbiprofeno también está contraindicado en pacientes con antecedentes de hemorragia gastrointestinal o perforación relacionada con un tratamiento previo con AINE.
Los pacientes con colitis ulcerosa activa o anamnésica, enfermedad de Crohn, úlcera péptica recurrente o hemorragia gastrointestinal no deben tomar flurbiprofeno (definido como dos o más episodios distintos de ulceración o hemorragia comprobada).
El flurbiprofeno está contraindicado en pacientes con insuficiencia cardíaca grave.
Tercer trimestre del embarazo
04.4 Advertencias especiales y precauciones de uso apropiadas
Efectos gastrointestinales
El flurbiprofeno debe administrarse con precaución a pacientes con antecedentes de úlcera péptica y otras enfermedades gastrointestinales, ya que estas afecciones pueden agravarse.
El riesgo de hemorragia, úlcera o perforación gastrointestinal es mayor con el aumento de la dosis de flurbiprofeno en pacientes con antecedentes de úlcera, especialmente si se complica con hemorragia y perforación y en los ancianos. Estos pacientes deben iniciar el tratamiento con la dosis más baja disponible.
Se han notificado hemorragias, úlceras o perforaciones gastrointestinales con todos los AINE en cualquier momento durante el tratamiento. Estos eventos adversos pueden ser fatales y pueden ocurrir con o sin síntomas de advertencia o con un historial previo de eventos gastrointestinales graves.
Los pacientes con antecedentes de enfermedad gastrointestinal, especialmente si son ancianos, deben informar cualquier síntoma abdominal inusual (especialmente hemorragia gastrointestinal) en las etapas iniciales del tratamiento.
Los pacientes de edad avanzada tienen una mayor frecuencia de reacciones adversas a los AINE, especialmente hemorragia y perforación gastrointestinal, que pueden ser mortales.
Las reacciones adversas pueden minimizarse utilizando la dosis efectiva más baja durante el tratamiento de menor duración posible necesario para controlar los síntomas (ver sección 4.2 y los párrafos siguientes sobre riesgos gastrointestinales y cardiovasculares).
Se debe considerar el uso concomitante de agentes protectores (misoprostol o inhibidores de la bomba de protones) para estos pacientes y también para pacientes que toman aspirina en dosis bajas u otros medicamentos que pueden aumentar el riesgo de eventos gastrointestinales (ver más abajo y la sección 4.5).
Cuando se produce hemorragia o ulceración gastrointestinal en pacientes que toman Froben, se debe interrumpir el tratamiento.
Efectos cardiovasculares y cerebrovasculares
Se requiere una supervisión e instrucción adecuadas en pacientes con antecedentes de hipertensión leve a moderada y / o insuficiencia cardíaca congestiva, ya que se ha informado retención de líquidos y edema en asociación con el tratamiento con AINE.
Los estudios clínicos y los datos epidemiológicos sugieren que el uso de algunos AINE, especialmente en dosis altas y para tratamientos a largo plazo, puede estar asociado con un aumento moderado del riesgo de eventos trombóticos arteriales como infarto de miocardio o accidente cerebrovascular. No hay datos suficientes para descarte un riesgo similar para el flurbiprofeno.
Los pacientes con hipertensión no controlada, insuficiencia cardíaca congestiva, cardiopatía isquémica establecida, enfermedad arterial periférica y / o enfermedad cerebrovascular solo deben tratarse con flurbiprofeno después de una cuidadosa consideración. Se deben hacer consideraciones similares antes de iniciar un tratamiento a largo plazo en pacientes con factores de riesgo de enfermedad cardiovascular (p. Ej., Hipertensión, hiperlipidemia, diabetes mellitus, tabaquismo).
El flurbiprofeno, al igual que otros AINE, puede inhibir la agregación plaquetaria y prolongar el tiempo de hemorragia.
Reacciones cutáneas
Muy raramente se han notificado reacciones cutáneas graves, algunas de ellas mortales, como dermatitis exfoliativa, síndrome de Stevens-Johnson y necrólisis epidérmica tóxica, asociadas al uso de AINE. Los pacientes parecen tener un mayor riesgo en las primeras etapas del tratamiento. El inicio de la reacción ocurre en la mayoría de los casos durante el primer mes de tratamiento. El flurbiprofeno debe suspenderse ante la primera aparición de erupción cutánea, lesiones de las mucosas o cualquier otro signo de hipersensibilidad.
Otras reacciones
Se debe tener precaución al iniciar el tratamiento con AINE como flurbiprofeno en pacientes con deshidratación considerable. Se debe tener especial precaución en el tratamiento de pacientes con función renal, cardíaca o hepática severamente reducida, ya que el uso de AINE puede conducir a un deterioro de la función renal. En tales pacientes, la dosis debe mantenerse lo más baja posible y la función renal debe reducirse. supervisado.
Se han notificado casos de broncoespasmo con flurbiprofeno en pacientes con antecedentes de asma bronquial.
Los efectos informados anteriormente se han informado en particular después de la administración de formulaciones a base de flurbiprofeno para uso sistémico.
A las dosis recomendadas, la posible ingestión de GARGANTA CONGELADA no causa ningún daño al paciente ya que estas dosis son muy inferiores a las de la dosis única del producto por vía sistémica.
El uso de GARGANTA FROBEN, especialmente si es prolongado, puede dar lugar a fenómenos de sensibilización o irritación local, en tales casos es necesario interrumpir el tratamiento y consultar al médico para establecer, si es necesario, una terapia adecuada.
No utilizar para tratamientos prolongados. Tras breves periodos de tratamiento sin resultados apreciables, consulte a su médico.
Tanto el enjuague bucal como el spray contienen alcohol etílico Para quienes realizan actividades deportivas, el uso de medicamentos que contengan alcohol etílico puede determinar pruebas de dopaje positivas en relación con los límites de concentración de alcohol indicados por algunas federaciones deportivas.
04.5 Interacciones con otros medicamentos y otras formas de interacción
Se debe prestar atención a los pacientes tratados con cualquiera de los medicamentos enumerados a continuación, ya que se han informado interacciones en algunos pacientes.
Diuréticos, inhibidores de la ECA y antagonistas de la angiotensina II: los AINE pueden reducir el efecto de los diuréticos y otros fármacos antihipertensivos. En algunos pacientes con insuficiencia renal (por ejemplo, pacientes deshidratados o pacientes de edad avanzada con insuficiencia renal), la coadministración de un inhibidor de la ECA o un antagonista de la angiotensina II y agentes que inhiben el sistema ciclooxigenasa puede conducir a un mayor deterioro de la función renal, incluyendo posible insuficiencia renal aguda, normalmente reversible Estas interacciones deben considerarse en pacientes que toman flurbiprofeno de forma concomitante con inhibidores de la ECA o antagonistas de la angiotensina II. Por tanto, la combinación debe administrarse con precaución, especialmente en pacientes de edad avanzada.
Los pacientes deben estar adecuadamente hidratados y se debe considerar la monitorización de la función renal después del inicio del tratamiento concomitante y de forma periódica a partir de entonces.
Glucósidos cardíacos: los AINE pueden exacerbar la insuficiencia cardíaca, reducir el grado de filtración glomerular y aumentar los niveles plasmáticos de glucósidos cardíacos.
Anticoagulantes, como warfarina: aumento del efecto anticoagulante.
Aspirina: al igual que con otros medicamentos que contienen AINE, generalmente no se recomienda la administración concomitante de flurbiprofeno y aspirina debido a la posibilidad de un aumento de los efectos secundarios.
Agentes antiagregantes: mayor riesgo de hemorragia gastrointestinal.
Inhibidores selectivos de la recaptación de serotonina (ISRS): mayor riesgo de hemorragia gastrointestinal.
Sales de litio: disminución de la remoción de litio.
Metotrexato: Se recomienda precaución en caso de administración concomitante de flurbiprofeno y metotrexato, ya que los AINE pueden aumentar los niveles de metotrexato.
Ciclosporinas: mayor riesgo de nefrotoxicidad con AINE.
Corticosteroides: mayor riesgo de úlcera gastrointestinal o hemorragia con los AINE.
Inhibidores de la cox-2 y otros AINE: debe evitarse el uso concomitante de otros AINE, incluidos los inhibidores selectivos de la ciclooxigenasa-2, debido a los posibles efectos aditivos.
Antibióticos quinolónicos: Los resultados de estudios en animales sugieren que los AINE pueden aumentar el riesgo de convulsiones asociadas con el uso de antibióticos quinolonas. Los pacientes que toman AINE y quinolonas pueden tener un mayor riesgo de desarrollar convulsiones.
Mifepristona: los AINE no deben tomarse durante 8-12 días después de la administración de mifepristona, ya que los AINE pueden reducir los efectos de la mifepristona.
Tacrolimus: Posible aumento del riesgo de nefrotoxicidad cuando se coadministra con AINE.
Zidovudina: mayor riesgo de toxicidad sanguínea cuando se coadministra con AINE. Existe evidencia de un mayor riesgo de hemartrosis y hematoma en pacientes hemofílicos infectados por el VIH tratados concomitantemente con zidovudina y otros AINE.
Las interacciones descritas anteriormente se han informado en particular después de la administración de formulaciones basadas en flurbiprofeno para uso sistémico.
A las dosis recomendadas de GARGANTA CONGELADA, no se han reportado interacciones con otros medicamentos u otros tipos. Sin embargo, informe a su médico si está tomando otros medicamentos.
04.6 Embarazo y lactancia
Fertilidad y embarazo
La inhibición de la síntesis de prostaglandinas puede afectar negativamente al embarazo y / o al desarrollo embrionario / fetal.
Los resultados de los estudios epidemiológicos sugieren un mayor riesgo de aborto espontáneo y malformaciones cardíacas y gastrosquisis después del uso de un inhibidor de la síntesis de prostaglandinas al comienzo del embarazo. El riesgo absoluto de malformaciones cardíacas aumentó de menos del 1% a aproximadamente el 1,5%. Se ha considerado que el riesgo aumenta con la dosis y la duración de la terapia En animales, se ha demostrado que la administración de inhibidores de la síntesis de prostaglandinas causa un aumento de la pérdida y mortalidad antes y después de la implantación.
Además, se ha informado una mayor incidencia de diversas malformaciones, incluidas las cardiovasculares, en animales que recibieron inhibidores de la síntesis de prostaglandinas durante el período organogenético.
Durante el primer y segundo trimestre del embarazo, no se debe administrar flurbiprofeno excepto en casos estrictamente necesarios.
Si una mujer que está intentando concebir o durante el primer y segundo trimestre del embarazo utiliza flurbiprofeno, la dosis y la duración del tratamiento deben mantenerse lo más bajas posible.
Durante el tercer trimestre del embarazo, todos los inhibidores de la síntesis de prostaglandinas pueden exponer al feto a:
• Toxicidad cardiopulmonar (con cierre prematuro del conducto arterial e hipertensión pulmonar);
• Disfunción renal, que puede progresar a insuficiencia renal con oligohidroamnios;
la madre y el recién nacido, al final del embarazo, para:
• Posible prolongación del tiempo de hemorragia, efecto antiplaquetario que puede ocurrir incluso a dosis muy bajas;
• Inhibición de las contracciones uterinas que resulta en un parto prolongado o retrasado.
En consecuencia, el flurbiprofeno está contraindicado durante el tercer trimestre del embarazo.
Hora de la comida
El flurbiprofeno se excreta en la leche materna; sin embargo, la cantidad excretada es solo una pequeña fracción de la dosis materna. No se recomienda la administración de flurbiprofeno en madres lactantes.
04.7 Efectos sobre la capacidad para conducir y utilizar máquinas
No afecta la capacidad para conducir y utilizar máquinas.
04.8 Efectos indeseables
Se han notificado las siguientes reacciones adversas, especialmente después de la administración de formulaciones para uso sistémico:
Trastornos del sistema sanguíneo y linfático.
Trombocitopenia, anemia aplásica y agranulocitosis
Trastornos del sistema inmunológico.
Anafilaxia, angioedema, reacción alérgica.
Desórdenes psiquiátricos
Depresión
Trastornos del sistema nervioso.
Mareos, accidentes cerebrovasculares, alteraciones visuales, neuritis óptica, migraña, parestesia, depresión, confusión, alucinaciones, vértigo, malestar general, fatiga y somnolencia.
Perturbaciones acústicas y laberínticas
Tinnitus
Desordenes cardiovasculares
Edema, hipertensión e insuficiencia cardíaca
Los estudios clínicos y los datos epidemiológicos sugieren que la ingesta de algunos AINE (especialmente en dosis altas y en el caso de un tratamiento a largo plazo) puede asociarse con un mayor riesgo de episodios trombóticos arteriales (p. Ej., Infarto de miocardio o accidente cerebrovascular).
Trastornos respiratorios, torácicos y mediastínicos
Reactividad del tracto respiratorio (asma, broncoespasmo y disnea)
Desórdenes gastrointestinales
Los eventos adversos observados con mayor frecuencia son de naturaleza gastrointestinal.
Se han notificado náuseas, vómitos, diarrea, flatulencia, estreñimiento, dispepsia, dolor abdominal, melena, hematemesis, estomatitis ulcerosa, hemorragia gastrointestinal y exacerbación de colitis y enfermedad de Crohn tras la administración de flurbiprofeno (ver sección Contraindicaciones). Se observaron con menor frecuencia gastritis, úlcera péptica, perforación y hemorragia ulcerosa. Puede producirse irritación local con los supositorios.
Muy raramente se han notificado casos de pancreatitis.
Trastornos de la piel y del tejido subcutáneo
Trastornos de la piel que incluyen erupción, prurito, urticaria, púrpura, angioedema y muy raramente dermatosis ampollosa (incluido el síndrome de Stevens-Johnson, necrólisis epidérmica tóxica y eritema multiforme).
Durante los ensayos clínicos con los parches de flurbiprofeno, las reacciones adversas notificadas con más frecuencia fueron reacciones cutáneas locales (que incluyen enrojecimiento, erupción cutánea, picor, erupción cutánea, entumecimiento y hormigueo); sin embargo, la incidencia fue baja (4,6%).
Trastornos de los riñones y del sistema urinario.
Nefrotoxicidad en diversas formas, incluida la nefritis intersticial y el síndrome nefrótico.
Al igual que con otros AINE, se han notificado casos raros de insuficiencia renal.
"Notificación de sospechas de reacciones adversas.
La notificación de sospechas de reacciones adversas que se produzcan después de la autorización del medicamento es importante, ya que permite un seguimiento continuo de la relación beneficio / riesgo del medicamento. Se ruega a los profesionales sanitarios que notifiquen cualquier sospecha de reacciones adversas a través del sistema nacional de notificación. "Dirección https: //www.aifa.gov.it/content/segnalazioni-reazioni-avverse ".
04.9 Sobredosis
Síntomas
Los síntomas de una sobredosis pueden incluir náuseas, vómitos e irritación gastrointestinal.
Tratamiento
El tratamiento debe incluir lavado gástrico y, si es necesario, corrección del cuadro de electrolitos séricos.
No existe un antídoto específico para el flurbiprofeno.
05.0 PROPIEDADES FARMACOLÓGICAS
05.1 Propiedades farmacodinámicas
Grupo farmacoterapéutico: fármacos antiinflamatorios y antirreumáticos,
estomatológico
CÓDIGO ATC: A01AD11
El flurbiprofeno posee propiedades analgésicas, antiinflamatorias y antipiréticas. Se cree que esto está relacionado con la capacidad del fármaco para inhibir la síntesis de prostaglandinas.
05.2 Propiedades farmacocinéticas
Después de la administración oral, el flurbiprofeno se absorbe fácilmente en el tracto gastrointestinal, y las concentraciones plasmáticas máximas ocurren aproximadamente 90 minutos después de la ingestión. En comparación con los comprimidos, la absorción de los supositorios puede ser más rápida, pero las concentraciones máximas en suero son menores.
El flurbiprofeno se une a proteínas en aproximadamente un 99% y tiene una vida media de eliminación de aproximadamente 3-4 horas. La tasa de excreción urinaria de flurbiprofeno y sus dos metabolitos principales, tanto en estado libre como conjugado, es similar tanto en estado libre como conjugado. las vías de administración oral y rectal Los patrones metabólicos también son similares desde un punto de vista cuantitativo para ambas vías de administración.
05.3 Datos preclínicos sobre seguridad
Las pruebas toxicológicas en animales han demostrado que el flurbiprofeno se tolera bien. Las pruebas de toxicidad aguda en varias especies animales, para administración oral, han demostrado que la DL50 del flurbiprofeno está entre 228-344 mg / kg. La administración de AINE a ratas preñadas puede resultar en restricción del conducto arterial fetal.
Los estudios clínicos a largo plazo no han mostrado efectos significativos sobre la función hepática o renal o sobre el sistema hematopoyético.
No hay más información sobre los datos preclínicos aparte de la ya informada en otra parte de este Resumen de las Características del Producto (ver sección 4.6).
06.0 INFORMACIÓN FARMACÉUTICA
06.1 Excipientes
Agua purificada, alcohol, azul patente VE 131, glicerol, esencia de menta, aceite de ricino hidrogenado 40-polioxietilenato, bicarbonato de potasio, sacarinato de sodio, sorbitol.
06.2 Incompatibilidad
No se conocen incompatibilidades químico-físicas del flurbiprofeno con otros compuestos.
06.3 Período de validez
• 2 años
• Validez después de la primera apertura: 1 año
06.4 Precauciones especiales de conservación
Enjuague bucal: este medicamento no requiere condiciones especiales de conservación. Aerosol bucal: este medicamento no requiere ninguna temperatura de almacenamiento particular; mantenga el frasco en el embalaje exterior para proteger el medicamento de la luz.
06.5 Naturaleza del envase primario y contenido del envase.
Enjuague bucal
• Caja que contiene una botella de PET oscura con tapón de polipropileno de 160 ml de solución
Spray de mucosa oral
Caja que contiene un frasco de vidrio blanco con bomba de microdosificación y dosificador de 15 ml de solución.
06.6 Instrucciones de uso y manipulación
GARGANTA CONGELADA 0,25% Aerosol bucal:
Gire la boquilla hacia la derecha o hacia la izquierda como se muestra, sin alterar el dispensador.
Presione el dispensador.
07.0 TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
BGP Products S.r.l., viale Giorgio Ribotta 11, 00144 - Roma
08.0 NÚMERO DE AUTORIZACIÓN DE COMERCIALIZACIÓN
• Enjuague bucal al 0,25% - Frasco de 160 ml - A.I.C.: N. 042822015
• Spray mucoso oral al 0,25% - Frasco de 15 ml - A.I.C .: n. 042822027
09.0 FECHA DE LA PRIMERA AUTORIZACIÓN O RENOVACIÓN DE LA AUTORIZACIÓN
• Enjuague bucal al 0,25% - Frasco de 160 ml: 27.04.1991
• Spray mucoso oral al 0,25% - Frasco de 15 ml: 11.11.1996
Renovación de la autorización: 01.06.2010