¿Qué es Silgard?
Silgard es una vacuna que consiste en una suspensión inyectable que contiene proteínas purificadas para cuatro tipos de virus del papiloma humano (tipos 6, 11, 16 y 18). Está disponible en viales o jeringas precargadas.
¿Para qué se utiliza Silgard?
Silgard se utiliza en pacientes a partir de los nueve años para proteger contra:
- lesiones precancerosas (proliferación celular anormal) en el área genital (cuello uterino, vulva o vagina) y cáncer de cuello uterino, causado por ciertos tipos cancerosos del virus del papiloma humano (VPH);
- Verrugas genitales externas (verrugas genitales) causadas por tipos específicos de VPH.
Silgard se administra de acuerdo con las recomendaciones oficiales.
La vacuna solo se podrá dispensar con receta médica.
¿Cómo se usa Silgard?
Silgard se administra a personas de al menos nueve años de edad, en tres dosis, con un intervalo de dos meses entre la primera y la segunda dosis y un intervalo de cuatro meses entre la segunda y la tercera dosis. Si se requiere un horario alternativo, la segunda dosis debe administrarse al menos un mes después de la primera y la tercera dosis al menos tres meses después de la segunda; todas las dosis deben administrarse dentro del período de un año. Se recomienda que una vez que se reciba la primera dosis de Silgard, el tratamiento se complete tomando las tres dosis. La vacuna se administra mediante inyección en un músculo, preferiblemente en el hombro o el muslo.
¿Cómo actúa Silgard?
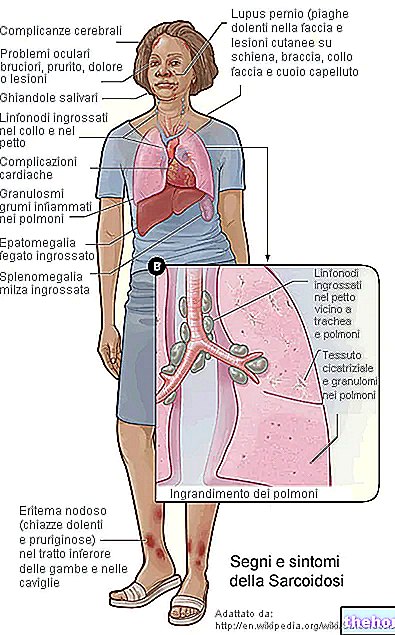
Los papilomavirus son virus que causan verrugas y crecimiento anormal de tejido. Hay más de 100 tipos de virus del papiloma, algunos de los cuales están asociados con cánceres de genitales. Los tipos 16 y 18 del VPH son responsables de aproximadamente el 70% de los cánceres de cuello uterino, mientras que los tipos 6 y 11 del VPH causan aproximadamente el 90% de las verrugas genitales.
Todos los virus del papiloma tienen una envoltura o "cápside", formada por proteínas llamadas "proteínas L1". Silgard contiene proteínas L1 purificadas para los tipos 6, 11, 16 y 18 del VPH; estos se producen mediante un método conocido como "tecnología del ADN recombinante", es decir, se obtienen mediante una levadura a la que se le ha dado un gen (ADN) que la hace capaz de producir proteínas L1. Las proteínas se recogen en "partículas similares a virus" (es decir, estructuras que se asemejan a los virus del VPH, de modo que el cuerpo no tiene dificultad para reconocerlas), incapaces de causar infección.
Cuando un paciente recibe la vacuna, el sistema inmunológico produce anticuerpos contra las proteínas L1. Después de la vacunación, el sistema inmunológico puede producir anticuerpos más rápidamente cuando se expone a virus reales. Esto ayudará a protegerse contra las enfermedades causadas por estos virus.
La vacuna también contiene un "adyuvante" (un compuesto que contiene aluminio) que estimula una mejor respuesta.
¿Qué tipo de estudios se han realizado con Silgard?
Silgard se ha estudiado en cuatro estudios principales en los que participaron un total de alrededor de 21.000 mujeres de entre 16 y 26 años. Silgard se comparó con un placebo (una vacuna ficticia). Los estudios analizaron el número de mujeres que desarrollaron lesiones genitales o verrugas atribuibles a la infección por VPH. Se observó a los participantes del estudio durante aproximadamente tres años después de la tercera dosis de la vacuna.
Estudios adicionales examinaron la capacidad de Silgard para prevenir la infección con los tipos 6, 11, 16 y 18 del VPH y lesiones genitales relacionadas en aproximadamente 4.000 mujeres de 24 a 45 años y observaron el desarrollo de anticuerpos contra estos tipos de VPH en aproximadamente 1.700 niñas y niños entre las edades de nueve y 15.
¿Qué beneficio ha demostrado Silgard durante los estudios?
Silgard fue eficaz contra las lesiones genitales precancerosas del cuello uterino, la vulva y la vagina, el cáncer de cuello uterino y las verrugas de los tipos 6, 11, 16 y 18 relacionadas con el VPH.
Al observar los resultados de los cuatro estudios en conjunto, entre las más de 8.000 mujeres vacunadas con Silgard que nunca habían contraído una infección por VPH tipo 6, 11, 16 o 18 en el pasado, una desarrolló una lesión precancerosa en el cuello uterino que podría han sido atribuibles al VPH tipo 16 o 18. En contraste, 85 de las más de 8,000 mujeres que recibieron placebo como vacuna tenían lesiones resultantes de estos tipos de VPH. Se encontró un efecto similar de Silgard cuando el análisis también incluyó lesiones cervicales debidas a los otros dos tipos de VPH (tipos 6 y 11).
En cuanto a las lesiones genitales externas atribuibles al VPH tipo 6, 11, 16 o 18 (incluidas las verrugas y las lesiones precancerosas de la vulva o la vagina), se examinaron juntos los resultados de tres de los estudios realizados. Dos de aproximadamente 8.000 mujeres en el grupo de Silgard desarrollaron verrugas genitales, mientras que no hubo informes de lesiones precancerosas de la vulva o la vagina. Por el contrario, en el grupo de placebo, se detectaron un total de 189 casos de lesiones genitales externas en unas 8.000 mujeres.
Los estudios también mostraron que Silgard proporcionó cierto nivel de protección contra las lesiones cervicales relacionadas con otros tipos cancerosos de VPH, incluido el tipo 31.
Estudios adicionales confirmaron la capacidad de Silgard para proteger contra las lesiones e infecciones por VPH en mujeres de 24 a 45 años. Los estudios también han demostrado que la vacuna estimula la producción de cantidades suficientes de anticuerpos contra el VPH en niñas y niños de entre nueve y 15 años.
¿Cuál es el riesgo asociado a Silgard?
Los efectos secundarios observados con mayor frecuencia asociados con Silgard en los estudios (en más de 1 de cada 10 pacientes) son pirexia (fiebre) y reacciones en el lugar de la inyección (enrojecimiento, dolor e hinchazón). Para obtener la lista completa de efectos secundarios detectados con Silgard, consulte el prospecto.
Silgard no debe administrarse a personas que puedan ser hipersensibles (alérgicas) al principio activo oa cualquiera de los demás componentes. Si aparecen signos de alergia después de una dosis de Silgard, se debe interrumpir la administración de las otras dosis de la vacuna. La vacunación debe posponerse en caso de pacientes con fiebre alta.
¿Por qué se ha aprobado Silgard?
El Comité de Medicamentos de Uso Humano (CHMP) decidió que los beneficios de Silgard son mayores que sus riesgos en la vacunación para prevenir lesiones genitales precancerosas (cervicales, vulvares y vaginales), cáncer de cuello uterino y lesiones genitales externas (condiloma acuminado) causadas por el VPH tipo 6 , 11, 16 y 18. Por tanto, el comité recomendó la concesión de una autorización de comercialización para Silgard.
Otras informaciones sobre Silgard:
El 20 de septiembre de 2006, la Comisión Europea otorgó a Merck Sharp & Dohme Ltd una "Autorización de comercialización" para Silgard, válida en toda la Unión Europea.
Para obtener la versión completa del EPAR de Silgard, haga clic aquí.
Para obtener más información sobre el tratamiento con Silgard, lea el prospecto (incluido con el EPAR) o consulte a su médico o farmacéutico.
Última actualización de este resumen: 07-2010.
La información sobre la vacuna contra el virus del papiloma Silgard publicada en esta página puede estar desactualizada o incompleta. Para un uso correcto de esta información, consulte la página de exención de responsabilidad e información útil.