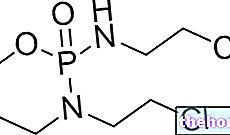
Ingredientes activos: Pregablin
Lyrica 25 mg cápsulas duras Lyrica 50 mg cápsulas duras Lyrica 75 mg cápsulas duras Lyrica 100 mg cápsulas duras Lyrica 150 mg cápsulas duras Lyrica 200 mg cápsulas duras Lyrica 225 mg cápsulas duras Lyrica 300 mg cápsulas duras
¿Por qué se usa Lyrica? ¿Para qué sirve?
Lyrica pertenece a un grupo de medicamentos que se utilizan para tratar la epilepsia, el dolor neuropático y el trastorno de ansiedad generalizada (TAG) en adultos.
Dolor neuropático periférico y central: Lyrica se usa para tratar el dolor crónico causado por daños en el sistema nervioso. Varias enfermedades pueden causar dolor neuropático periférico, como diabetes o herpes zóster. Las sensaciones de dolor pueden describirse como calor, ardor, pulsaciones, dolores de relámpago, dolores punzantes, dolores agudos, calambres, dolor, hormigueo, entumecimiento, escozor. Periférico y central El dolor neuropático también puede estar asociado con cambios de humor, alteraciones del sueño y fatiga (cansancio) y puede afectar la actividad física y social y la calidad de vida en general.
Epilepsia: Lyrica se utiliza para tratar algunas formas de epilepsia en adultos (convulsiones parciales con o sin generalización secundaria). Su médico le recetará Lyrica para ayudarlo a tratar la epilepsia cuando el tratamiento continuo no controle la situación. Deberá tomar Lyrica además del tratamiento que ya está recibiendo. Lyrica no se usa solo, pero siempre debe combinarse con otros tratamientos antiepilépticos.
Trastorno de ansiedad generalizada: Lyrica se utiliza para el tratamiento del trastorno de ansiedad generalizada (TAG). Los síntomas del trastorno de ansiedad generalizada se caracterizan por una ansiedad y preocupación excesivas y prolongadas que son difíciles de controlar. El Trastorno de Ansiedad Generalizada también puede causar inquietud o sensación de tensión o nervios en la piel, fatiga fácil, dificultad para concentrarse o lapsus de memoria, irritabilidad, tensión muscular o alteraciones del sueño. Estas condiciones son diferentes al estrés y las tensiones de la vida cotidiana.
Precauciones de uso Lo que necesita saber antes de tomar Lyrica
No tome Lyrica
si es alérgico a la pregabalina oa cualquiera de los demás componentes de este medicamento (incluidos en la sección 6).
Advertencias y precauciones
- Se han notificado síntomas que sugieren reacciones alérgicas en algunos pacientes que toman Lyrica. Estos síntomas incluyen hinchazón de la cara, labios, lengua y garganta, así como una erupción generalizada. Si se produce alguna de estas reacciones, póngase en contacto con su médico de inmediato.
- Lyrica se ha asociado con mareos y somnolencia que pueden aumentar la incidencia de lesiones accidentales (caídas) en los ancianos. Por lo tanto, debe tener cuidado hasta que se familiarice con los efectos que puede tener el medicamento.
- Lyrica puede causar visión borrosa o pérdida de la visión u otros cambios en la visión, muchos de los cuales son temporales. Si se produce algún cambio en la visión, debe comunicarse con su médico de inmediato.
- Algunos pacientes con diabetes que aumentan de peso durante el tratamiento con pregabalina pueden necesitar cambiar sus medicamentos para la diabetes.
- Algunos efectos secundarios, como la somnolencia, pueden ser más frecuentes porque los pacientes con lesión de la médula espinal pueden estar siendo tratados con otros medicamentos para tratar, por ejemplo, el dolor o la espasticidad, que tienen efectos secundarios similares a los de la pregabalina y la gravedad de estos efectos puede aumentar cuando estos medicamentos se toman juntos.
- Ha habido informes de insuficiencia cardíaca en algunos pacientes que toman Lyrica; estos pacientes eran en su mayoría ancianos con enfermedad cardiovascular. Si tiene antecedentes de enfermedad cardiovascular, debe informar a su médico antes de iniciar el tratamiento con este medicamento.
- Ha habido informes de insuficiencia renal en algunos pacientes que toman Lyrica. Si durante el tratamiento con Lyrica nota una disminución en la micción, debe informar a su médico, ya que interrumpir el uso de este medicamento puede mejorar esta afección.
- Un pequeño número de pacientes en tratamiento con medicamentos antiepilépticos como Lyrica han tenido pensamientos de matar y hacerse daño (hacerse daño a sí mismos). Si tiene alguno de estos pensamientos, comuníquese con su médico de inmediato.
- Cuando Lyrica se usa junto con otros medicamentos que pueden causar estreñimiento (como algunos tipos de analgésicos), pueden ocurrir problemas gastrointestinales (por ejemplo, estreñimiento, intestino bloqueado o paralizado). Informe a su médico si tiene estreñimiento, especialmente si tiene este problema.
- Antes de tomar este medicamento, dígale a su médico si tiene antecedentes de dependencia del alcohol o abuso o dependencia de cualquier droga No tome más medicamento de lo recetado.
- Ha habido informes de convulsiones al tomar Lyrica o poco después de suspenderlo. Si experimenta convulsiones, comuníquese con su médico de inmediato.
- Ha habido casos de función cerebral disminuida (encefalopatía) en algunos pacientes que toman LYRICA cuando tienen otras afecciones. Informe a su médico si tiene antecedentes de cualquier otra afección médica grave, incluida una enfermedad hepática o renal.
Niños y adolescentes
No se ha establecido la seguridad y eficacia de pregabalina en niños y adolescentes (menores de 18 años) y, por tanto, no se debe utilizar pregabalina en este grupo de edad.
Interacciones ¿Qué medicamentos o alimentos pueden cambiar el efecto de Lyrica?
Otros medicamentos y Lyrica
Informe a su médico o farmacéutico si está tomando, ha tomado recientemente o podría tener que tomar cualquier otro medicamento. Lyrica y otros medicamentos pueden afectarse entre sí (interacción). Cuando Lyrica se toma junto con otros medicamentos, puede potenciar los efectos secundarios observados con estos medicamentos, incluyendo insuficiencia respiratoria y coma. La intensidad de los mareos, la somnolencia y la disminución de la concentración pueden aumentar si se toma Lyrica junto con otros medicamentos que contengan: Oxicodona - (utilizado como analgésico) Lorazepam - (utilizado para tratar la ansiedad) El alcohol Lyrica se puede tomar al mismo tiempo que los anticonceptivos orales. .
Toma de Lyrica con alimentos y bebidas
Las cápsulas de Lyrica se pueden tomar con o sin alimentos. Es aconsejable no beber alcohol mientras esté tomando Lyrica.
Embarazo y lactancia
Lyrica no debe tomarse durante el embarazo a menos que su médico le indique lo contrario. Las mujeres en edad fértil deben utilizar un método anticonceptivo eficaz. Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico o farmacéutico antes de utilizar este medicamento. Se recomienda que no amamante mientras toma Lyrica ya que no se sabe si Lyrica puede pasar a la leche materna. Consulte a su médico o farmacéutico antes de tomar cualquier medicamento durante la lactancia.
Conducción y uso de máquinas
Lyrica puede causar mareos, somnolencia y disminución de la concentración. No debe conducir, operar maquinaria compleja o participar en actividades potencialmente peligrosas hasta que esté seguro de que este medicamento afecta su capacidad para realizar estas actividades.
Lyrica contiene lactosa monohidrato
Si su médico le ha dicho que padece una intolerancia a ciertos azúcares, consulte con él antes de tomar este medicamento.
Contenido del envase e información adicional Composición de Lyrica
El ingrediente activo es pregabalina. Cada cápsula dura contiene 25 mg, 50 mg, 75 mg, 100 mg, 150 mg, 200 mg, 225 mg o 300 mg de pregabalina.
Los demás componentes son: lactosa monohidrato, almidón de maíz, talco, gelatina, dióxido de titanio (E171), lauril sulfato de sodio, sílice coloidal anhidra, tinta negra (contiene goma laca, óxido de hierro negro (E172)), propilenglicol, hidróxido de potasio) y agua purificada.
Las cápsulas de 75 mg, 100 mg, 200 mg, 225 mg y 300 mg también contienen óxido de hierro rojo (E172).
Lyrica está disponible en ocho envases de PVC con una cara recubierta de aluminio: un envase de 14 cápsulas que contienen 1 blíster, un envase de 21 cápsulas que contienen 1 blíster, un envase de 56 cápsulas que contienen 4 blísteres, un envase de 70 cápsulas que contienen 5 blísteres, una envase de 84 cápsulas que contienen 4 blísteres, un envase de 100 cápsulas que contienen 10 blísteres, un envase de 112 (2 x 56) cápsulas y un envase de 100 cápsulas x 1 en forma de blísters unidosis perforados.
Lyrica también está disponible en frascos de HDPE que contienen 200 cápsulas para concentraciones de 75, 150 y 300 mg.
Es posible que no se comercialicen todos los tamaños de envases.
Dosis, método y momento de administración Cómo usar Lyrica: Posología
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico. En caso de duda, consulte a su médico o farmacéutico. Su médico determinará la dosis adecuada para usted. Lyrica es solo para uso oral.
Dolor neuropático periférico y central, epilepsia o trastorno de ansiedad generalizada:
- Tome la cantidad de cápsulas recetadas por su médico.
- La dosis adecuada para usted y su afección generalmente varía entre 150 mg y 600 mg por día.
- Su médico le indicará que tome Lyrica dos o tres veces al día. Si toma este medicamento dos veces al día, tome Lyrica una vez por la mañana y otra por la noche, siempre aproximadamente a la misma hora. Si toma este medicamento tres veces al día, tome Lyrica una vez por la mañana, una vez por la tarde y otra por la noche, siempre aproximadamente a la misma hora.
Si estima que el efecto de Lyrica es demasiado fuerte o débil, comuníqueselo a su médico o farmacéutico. Si es una persona de edad avanzada (mayor de 65 años), necesitará tomar Lyrica normalmente, excepto si tiene problemas renales. Su médico puede recetarle una concentración diferente y / o una dosis diferente si tiene problemas renales. Trague la cápsula entera con el agua y continúe tomando Lyrica hasta que su médico le indique que deje de tomarla.
Sobredosis Qué hacer si ha tomado demasiado Lyrica
Si toma más Lyrica del que debiera
Póngase en contacto con su médico inmediatamente o acuda al hospital más cercano de inmediato. Lleve consigo el envase de las cápsulas de Lyrica. Puede sentirse somnoliento, confundido, agitado e inquieto, ya que ha tomado más LYRICA del que debiera.
Si olvidó tomar Lyrica
Es importante que tome sus cápsulas de Lyrica regularmente a la misma hora todos los días. Si olvidó tomar una dosis, tómela tan pronto como recuerde que no la ha tomado a menos que sea el momento de su próxima dosis. En este caso, simplemente tome la siguiente dosis según lo planeado. No tome una dosis doble para compensar las dosis olvidadas.
Si deja de tomar Lyrica
No deje de tomar Lyrica a menos que su médico se lo indique. Si se interrumpe el tratamiento, debe retirarse gradualmente durante al menos 1 semana Debe tener en cuenta que pueden producirse algunos efectos secundarios después de interrumpir el tratamiento con Lyrica a corto y largo plazo. Estos incluyen alteraciones del sueño, dolores de cabeza, náuseas, ansiedad, diarrea, síntomas de la gripe, convulsiones, nerviosismo, depresión, dolor, sudoración y mareos. Estos síntomas pueden ocurrir con mayor frecuencia o gravedad si ha estado tomando Lyrica durante un período de tiempo más prolongado. Si tiene más preguntas sobre el uso de este medicamento, consulte a su médico o farmacéutico.
Efectos secundarios ¿Cuáles son los efectos secundarios de Lyrica?
Como todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Efectos adversos muy frecuentes que pueden afectar a más de 1 de cada 10 personas:
- Mareos, somnolencia, dolor de cabeza
Efectos adversos frecuentes que pueden afectar a más de 1 de cada 100 personas:
- Apetito incrementado
- Sensación de excitación, confusión, desorientación, disminución del interés sexual,
- irritabilidad
- Alteración de la atención, torpeza, deterioro de la memoria, pérdida de memoria,
- temblor, dificultad para hablar, sensación de hormigueo, entumecimiento, sedación, letargo,
- insomnio, sensación de agotamiento extraño,
- Visión borrosa, visión doble.
- Vértigo, alteraciones del equilibrio, caídas.
- Sequedad de boca, estreñimiento, vómitos, flatulencia, diarrea, náuseas e hinchazón,
- Dificultad para la erección
- Hinchazón del cuerpo, incluidos manos y pies.
- Sensación de intoxicación, marcha anormal.
- Aumento de peso
- Calambres musculares, dolor en las articulaciones, dolor de espalda, dolor en las extremidades.
- Dolor de garganta
Efectos adversos poco frecuentes que pueden afectar a más de 1 de cada 1.000 personas:
- Pérdida de apetito, pérdida de peso, niveles bajos de azúcar en sangre, niveles altos de azúcar en sangre.
- Percepción alterada de uno mismo, inquietud, depresión, agitación, cambios de humor, dificultad para encontrar palabras, alucinaciones, sueños alterados, ataques de pánico, apatía, agresión, estado de ánimo eufórico, deterioro mental, dificultad para pensar, aumento del interés sexual, problemas con la sexualidad, incluida la incapacidad. alcanzar el orgasmo, eyaculación retardada "
- Cambios en la visión, anomalías en el movimiento de los ojos, cambios en la visión que incluyen visión tubular, destellos de luz, movimientos espasmódicos, reflejos reducidos, aumento de la actividad, mareos al estar de pie, sensibilidad en la piel, pérdida del gusto, sensación de ardor, temblor durante el movimiento, disminución del conocimiento, pérdida del conocimiento. , desmayos, aumento de la sensibilidad al ruido, malestar
- Sequedad ocular, hinchazón ocular, dolor ocular, debilidad ocular, ojos llorosos, irritación ocular.
- Alteraciones del ritmo cardíaco, aumento de la frecuencia cardíaca, presión arterial baja, presión arterial alta, cambios en los latidos del corazón, insuficiencia cardíaca,
- Trastornos vasomotores (enrojecimiento), sofocos
- Dificultad para respirar, sequedad nasal, congestión nasal,
- Aumento de la producción de saliva, acidez de estómago, entumecimiento alrededor de la boca.
- Sudoración, sarpullido, escalofríos, fiebre. Espasmos musculares, hinchazón de las articulaciones, rigidez muscular, dolor que incluye dolor muscular, dolor de cuello
- Dolor en los senos
- Micción difícil o dolorosa, incontinencia.
- Debilidad, sed, opresión en el pecho. Cambios en los resultados de los análisis de sangre y las pruebas de función hepática (aumento de la creatina fosfoquinasa en sangre, aumento de la alanina aminotransferasa, aumento de la aspartato aminotransferasa, disminución del recuento de plaquetas, neutropenia, aumento de la creatina en sangre, disminución del potasio en sangre.
- Hipersensibilidad, hinchazón facial, picazón, urticaria, secreción nasal, hemorragia nasal, tos, ronquidos,
- Ciclos menstruales dolorosos
- Manos y pies fríos
Efectos adversos raros que pueden afectar a menos de 1 de cada 1.000 personas:
- Sentido del olfato alterado, sensación de oscilación del campo visual, percepción alterada de la profundidad, brillo visual, pérdida de la visión
- Pupilas dilatadas, estrabismo,
- Sudores fríos, opresión en la garganta, hinchazón de la lengua
- Inflamación del páncreas
- Dificultad para tragar
- Movimiento corporal lento o reducido
- Dificultad para escribir correctamente
- Aumento de líquido en el abdomen
- Presencia de líquido en los pulmones.
- Convulsiones
- Cambios en el electrocardiograma (ECG) que corresponden a alteraciones del ritmo cardíaco.
- Daño muscular
- Secreción mamaria, crecimiento anormal de las mamas, crecimiento de las mamas en los hombres
- Ciclos menstruales interrumpidos
- Insuficiencia renal, disminución del volumen de orina, retención urinaria,
- Reducción del recuento de glóbulos blancos
- Comportamiento inapropiado
- Reacciones alérgicas (que pueden incluir dificultad para respirar, inflamación de los ojos (queratitis) y una reacción cutánea grave caracterizada por erupción, ampollas, descamación de la piel y dolor.
Si experimenta hinchazón de la cara o la lengua o si la piel se enrojece y comienzan a formarse ampollas o se descama la piel, debe comunicarse con su médico de inmediato.
Algunos efectos secundarios, como la somnolencia, pueden ser más frecuentes porque los pacientes con lesión de la médula espinal pueden estar siendo tratados con otros medicamentos para tratar, por ejemplo, el dolor o la espasticidad, que tienen efectos secundarios similares a los de la pregabalina y la gravedad de estos efectos puede aumentar cuando estos medicamentos se toman juntos.
Si experimenta efectos adversos, consulte a su médico o farmacéutico, incluidos los posibles efectos adversos que no aparecen en este prospecto.
Caducidad y retención
Mantenga este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en la caja o frasco La fecha de caducidad se refiere al último día del mes.
Este medicamento no requiere condiciones especiales de conservación.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que no necesita, ya que esto ayudará a proteger el medio ambiente.
Prospecto fuente: AIFA (Agencia Italiana de Medicamentos). Contenido publicado en enero de 2016. Es posible que la información presente no esté actualizada.
Para tener acceso a la versión más actualizada, es recomendable acceder al sitio web de la AIFA (Agencia Italiana de Medicamentos). Descargo de responsabilidad e información útil.
01.0 NOMBRE DEL MEDICAMENTO
LYRICA 100 mg CÁPSULAS DURAS
02.0 COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Cada cápsula dura contiene 100 mg de pregabalina.
Excipientes
Cada cápsula dura también contiene 11 mg de lactosa monohidrato.
Para consultar la lista completa de excipientes, ver sección 6.1.
03.0 FORMA FARMACÉUTICA
Cápsula dura.
Cápsula marcada con tinta negra "Pfizer" en la tapa y "PGN 100" en el cuerpo.
04.0 INFORMACIÓN CLÍNICA
04.1 Indicaciones terapéuticas
Dolor neuropático
Lyrica está indicado para el tratamiento del dolor neuropático periférico y central en adultos.
Epilepsia
Lyrica está indicado como terapia complementaria en adultos con convulsiones parciales con o sin generalización secundaria.
Trastorno de ansiedad generalizada
Lyrica está indicado para el tratamiento del trastorno de ansiedad generalizada (TAG) en adultos.
04.2 Posología y forma de administración
La dosis varía de 150 a 600 mg por día, dividida en dos o tres administraciones.
Dolor neuropático
El tratamiento con pregabalina se puede iniciar con una dosis de 150 mg al día en dos o tres dosis divididas. Según la respuesta y la tolerabilidad del paciente individual, la dosis puede aumentarse a 300 mg por día después de un intervalo de 3 a 7 días y, si es necesario, a una dosis máxima de 600 mg por día después de un intervalo adicional.7 días.
Epilepsia
El tratamiento con pregabalina se puede iniciar con una dosis de 150 mg al día en dos o tres dosis divididas. Según la respuesta y la tolerabilidad del paciente individual, la dosis puede aumentarse a 300 mg por día después de 1 semana. La dosis máxima de 600 mg por día se puede alcanzar después de una semana adicional.
Trastorno de ansiedad generalizada
La dosis es de 150 a 600 mg al día para administrar en dos o tres dosis. La necesidad de tratamiento debe reevaluarse periódicamente.
El tratamiento con pregabalina se puede iniciar con una dosis de 150 mg al día. Según la respuesta y la tolerabilidad del paciente individual, la dosis puede aumentarse a 300 mg por día después de 1 semana. Después de una semana más, la dosis se puede aumentar a 450 mg por día.
La dosis máxima de 600 mg por día se puede alcanzar después de una semana adicional.
Interrupción del tratamiento con pregabalina
De acuerdo con la práctica clínica actual, si se debe suspender la pregabalina, independientemente de la indicación, se recomienda suspender el tratamiento gradualmente durante al menos 1 semana (ver secciones 4.4 y 4.8).
Población especial
Pacientes con insuficiencia renal
La pregabalina se elimina de la circulación sistémica principalmente por excreción renal en forma de fármaco inalterado. Dado que el aclaramiento de pregabalina es directamente proporcional al aclaramiento de creatinina (ver sección 5.2), la reducción de la dosis de pregabalina en pacientes con insuficiencia renal debe individualizarse en función del aclaramiento de creatinina (CLcr), como se indica en la Tabla 1, aplicando la siguiente fórmula:
La pregabalina se elimina eficazmente del plasma mediante hemodiálisis (50% del fármaco en 4 horas). Para los pacientes sometidos a hemodiálisis, la dosis diaria de pregabalina debe ajustarse en función de la función renal. Además de la dosis diaria, se debe administrar una dosis adicional de pregabalina inmediatamente después de cada sesión de diálisis de 4 horas (ver Tabla 1).
Tabla 1. Ajuste de la dosis de pregabalina en función de la función renal
TID = Tres administraciones
BID = Dos administraciones
* La dosis diaria total (mg / día) debe dividirse según las indicaciones del régimen de dosificación para obtener la dosis única prevista en mg.
+ La dosis suplementaria es una dosis adicional única
Uso en pacientes con insuficiencia hepática.
No es necesario un ajuste de dosis en pacientes con insuficiencia hepática (ver sección 5.2).
Población pediátrica
Aún no se ha establecido la seguridad y eficacia en niños menores de 12 años y adolescentes (12-17 años) No hay datos disponibles.
Uso en ancianos (mayores de 65 años)
Puede ser necesaria una reducción de la dosis de pregabalina en pacientes de edad avanzada debido a la función renal disminuida (ver pacientes con insuficiencia renal).
Método de administración
Lyrica se puede tomar con o sin alimentos.
LYRICA es solo para uso oral.
04.3 Contraindicaciones
Hipersensibilidad al principio activo oa alguno de los excipientes.
04.4 Advertencias especiales y precauciones de uso apropiadas
Pacientes diabéticos
Según la práctica clínica actual, en algunos pacientes diabéticos que aumentan de peso durante el tratamiento con pregabalina, puede ser necesario ajustar la dosis de los medicamentos hipoglucemiantes.
Reacciones hipersensibles
Después de la comercialización se han notificado reacciones de hipersensibilidad, incluidos casos de angioedema. El tratamiento con pregabalina debe interrumpirse inmediatamente en presencia de síntomas de angioedema como hinchazón de la cara, hinchazón perioral o hinchazón del tracto respiratorio superior.
Mareos, somnolencia, pérdida del conocimiento, confusión y deterioro mental.
El tratamiento con pregabalina se ha asociado con mareos y somnolencia que pueden aumentar el riesgo de lesiones accidentales (caídas) en pacientes de edad avanzada. También se han notificado casos de inconsciencia, confusión y deterioro mental. Por lo tanto, se debe advertir a los pacientes que tengan precaución hasta que estén familiarizados con los efectos potenciales de este medicamento.
Efectos relacionados con la vista
En los ensayos no controlados, se notificó visión borrosa en una mayor proporción de pacientes tratados con pregabalina que en pacientes tratados con placebo y se resolvió en la mayoría de los casos con el tratamiento continuado. En los ensayos clínicos en los que se realizó una prueba oftalmológica, la incidencia de disminución de la agudeza visual y cambios en el campo visual fue mayor en los pacientes tratados con pregabalina que en los pacientes tratados con placebo; por otro lado, la incidencia de alteraciones detectadas en el examen fundoscópico fue mayor en los pacientes tratados con placebo (ver sección 5.1).
También se han notificado reacciones adversas visuales, incluida la pérdida de visión, visión borrosa u otras alteraciones de la agudeza visual, muchas de ellas transitorias, en el entorno poscomercialización. La interrupción del tratamiento con pregabalina puede dar lugar a una resolución o mejora de estos síntomas de la visión.
Insuficiencia renal
Se han notificado casos de insuficiencia renal y, en algunos casos, la interrupción de la pregabalina ha demostrado que esta reacción adversa es reversible.
Interrupción del tratamiento con otros medicamentos antiepilépticos.
No hay datos suficientes de que una vez que se haya logrado el control de las convulsiones con la terapia adicional de pregabalina, se pueda interrumpir el tratamiento concomitante con otros medicamentos antiepilépticos y mantener la monoterapia con pregabalina.
Síntomas de abstinencia
En algunos pacientes, se han observado síntomas de abstinencia tras la interrupción del tratamiento a corto y largo plazo con pregabalina. Se han notificado los siguientes acontecimientos: insomnio, dolor de cabeza, náuseas, ansiedad, diarrea, síndrome gripal, nerviosismo, depresión, dolor, convulsiones, hiperhidrosis y mareos. Se debe informar a los pacientes de este hecho antes de iniciar el tratamiento.
Las convulsiones, incluido el estado epiléptico y las convulsiones de gran mal, pueden ocurrir durante el tratamiento con pregabalina o poco después de interrumpir el tratamiento.
Con respecto a la interrupción del tratamiento a largo plazo con pregabalina, no existen datos sobre la incidencia y la gravedad de los síntomas de abstinencia en relación con la duración del tratamiento y la dosis de pregabalina.
Insuficiencia cardíaca congestiva
Ha habido informes posteriores a la comercialización de insuficiencia cardíaca congestiva en algunos pacientes que toman pregabalina. Estas reacciones se observan principalmente en pacientes de edad avanzada con enfermedad cardiovascular tratados con pregabalina para el dolor neuropático. La pregabalina debe usarse con precaución en estos pacientes. La interrupción del tratamiento con pregabalina puede resolver esta afección.
Tratamiento del dolor neuropático central debido a una lesión espinal
En el tratamiento del dolor neuropático central debido a una lesión de la médula espinal, aumenta la incidencia de reacciones adversas en general, reacciones adversas del sistema nervioso central y somnolencia en particular, lo que puede atribuirse a un efecto adicional causado por medicamentos concomitantes (p. Ej. agentes espásticos) necesarios para esta afección Esto debe tenerse en cuenta cuando se prescriba pregabalina en esta afección.
Concepción y comportamiento suicida
Se han notificado casos de ideación y comportamiento suicida en pacientes que reciben medicamentos antiepilépticos en sus distintas indicaciones. Un metanálisis de ensayos aleatorios controlados con placebo con fármacos antiepilépticos también encontró un riesgo levemente mayor de ideación y comportamiento suicida. Se desconoce el mecanismo de este riesgo y los datos disponibles no excluyen la posibilidad de un aumento del riesgo durante el tratamiento con pregabalina.
Por tanto, se debe monitorizar a los pacientes para detectar signos de ideación y comportamiento suicidas y se debe considerar el tratamiento adecuado. Se debe advertir a los pacientes (y cuidadores) que consulten a su médico si surgen signos de ideación o comportamiento suicida.
Función reducida del tracto gastrointestinal inferior
Se han notificado acontecimientos relacionados con la disminución de la función gastrointestinal (p. Ej., Obstrucción intestinal, íleo paralítico, estreñimiento) cuando se coadministra pregabalina con medicamentos que pueden causar estreñimiento, como los analgésicos opioides. Cuando se utilizan pregabalina y opioides en combinación, se pueden considerar medidas preventivas para el estreñimiento (especialmente en mujeres y ancianos).
Casos de abuso
Se han informado casos de abuso. Se debe tener precaución en pacientes con antecedentes de abuso y, en estos casos, se debe monitorear al paciente para detectar la posible aparición de síntomas de abuso de pregabalina.
Encefalopatía
Se han notificado casos de encefalopatía, principalmente en pacientes con afecciones subyacentes que pueden precipitar una "encefalopatía".
Intolerancia a la lactosa
LYRICA contiene lactosa monohidrato. Los pacientes con intolerancia hereditaria a galactosa, deficiencia de lactasa de Lapp o problemas de absorción de glucosa o galactosa no deben tomar este medicamento.
04.5 Interacciones con otros medicamentos y otras formas de interacción
Dado que la pregabalina se excreta principalmente sin cambios en la orina, sufre un metabolismo insignificante en humanos (in vitro y no se une a las proteínas plasmáticas, es poco probable que cause o experimente interacciones farmacocinéticas).
Educación en vivo y análisis farmacocinético poblacional
Como resultado, en los estudios en vivo no se observaron interacciones farmacocinéticas clínicamente relevantes entre pregabalina y fenitoína, carbamazepina, ácido valproico, lamotrigina, gabapentina, lorazepam, oxicodona o etanol. El análisis farmacocinético poblacional indicó que los antidiabéticos orales, diuréticos, insulina, fenobarbital, tiagabina y topiramato no tuvieron un efecto clínicamente significativo sobre el aclaramiento de pregabalina.
Anticonceptivos orales noretisterona y / o etinilestradiol
La administración concomitante de pregabalina con los anticonceptivos orales noretisterona y / o etinilestradiol no afecta la farmacocinética de las dos sustancias. estado estable.
Etanol, lorazepam y oxicodona
La pregabalina puede potenciar los efectos del etanol y el lorazepam. En ensayos clínicos controlados, múltiples dosis orales de pregabalina administradas con oxicodona, lorazepam o etanol no tuvieron un efecto clínicamente importante sobre la respiración. Ha habido informes posteriores a la comercialización de insuficiencia respiratoria y coma en pacientes que toman pregabalina y otros medicamentos depresores del SNC. La pregabalina parece tener un efecto aditivo sobre la función cognitiva y la función motora dañadas por la 'oxicodona.
Interacciones en pacientes ancianos
No se han realizado estudios específicos de interacciones farmacodinámicas en voluntarios ancianos sanos. Los estudios de interacciones solo se han realizado en adultos.
04.6 Embarazo y lactancia
Mujeres en edad fértil / Anticoncepción en hombres y mujeres
Como aún no se conoce el riesgo potencial en los hombres, las mujeres en edad fértil deben utilizar un método anticonceptivo eficaz.
El embarazo
No existen datos suficientes sobre el uso de pregabalina en mujeres embarazadas.
Los estudios en animales han mostrado toxicidad para la reproducción (ver sección 5.3). Se desconoce el riesgo potencial para los seres humanos. Lyrica no debe usarse durante el embarazo a menos que sea claramente necesario (si el beneficio para la madre supera claramente el riesgo potencial para el feto).
Hora de la comida
Se desconoce si la pregabalina se excreta en la leche materna; sin embargo, está presente en la leche de ratas. Por lo tanto, se recomienda no amamantar durante el tratamiento con pregabalina.
Fertilidad
No hay datos clínicos sobre los efectos de la pregabalina en mujeres en edad fértil.
En un estudio clínico para evaluar el efecto de la pregabalina sobre la motilidad de los espermatozoides, se expuso a pacientes varones sanos a una dosis de pregabalina de 600 mg / día. Después de 3 meses de tratamiento no hubo evidencia de efectos sobre la motilidad de los espermatozoides.
Un estudio de fertilidad en ratas hembra ha mostrado reacciones reproductivas adversas.
El estudio de fertilidad en ratas macho mostró reacciones adversas de reproducción y desarrollo. Se desconoce la relevancia clínica de estas enfermedades. (ver párrafo 5.3)
04.7 Efectos sobre la capacidad para conducir y utilizar máquinas
Lyrica puede tener una influencia mínima o moderada sobre la capacidad para conducir y utilizar máquinas. Lyrica puede provocar mareos y somnolencia y, por tanto, puede afectar a la capacidad para conducir o utilizar máquinas. Se debe advertir a los pacientes que no conduzcan, operen maquinaria compleja o que realicen otras actividades potenciales. actividades peligrosas hasta que se sepa si este medicamento afecta la capacidad para realizar estas actividades.
04.8 Efectos indeseables
El programa clínico de pregabalina involucró a más de 8900 pacientes tratados con pregabalina; más de 5.600 de estos pacientes se inscribieron en ensayos clínicos doble ciego controlados con placebo. Las reacciones adversas notificadas con más frecuencia fueron mareos y somnolencia. Las reacciones adversas fueron generalmente de intensidad leve a moderada. En todos los estudios controlados, la tasa de interrupción de las reacciones adversas fue del 12% para los pacientes que tomaban pregabalina y del 5% para los que tomaban placebo. Las reacciones adversas más frecuentes que llevaron a la interrupción de la pregabalina fueron mareos y somnolencia.
La siguiente tabla enumera todas las reacciones adversas que ocurrieron con una "incidencia mayor que el placebo y en más de un paciente y están clasificadas por sistema de clasificación de órganos y frecuencia (muy frecuentes (≥ 1/10), frecuentes (≥ 1/100,
Las reacciones adversas enumeradas también pueden estar asociadas con la enfermedad subyacente y / o el uso de medicamentos concomitantes.
En el tratamiento del dolor neuropático central debido a una lesión de la médula espinal, aumenta la incidencia de reacciones adversas en general, reacciones del SNC y, en particular, somnolencia (ver sección 4.4).
Otras reacciones notificadas durante la experiencia postcomercialización se incluyen en una frecuencia desconocida en cursiva en la lista siguiente.
En algunos pacientes, se han observado síntomas de abstinencia tras la interrupción del tratamiento a corto y largo plazo con pregabalina. Se han notificado las siguientes reacciones: insomnio, dolor de cabeza, náuseas, ansiedad, diarrea, síndrome gripal, convulsiones, nerviosismo, depresión, dolor, hiperhidrosis y mareos. Se debe informar a los pacientes de este hecho antes de iniciar el tratamiento.
Con respecto a la interrupción del tratamiento a largo plazo con pregabalina, no existen datos sobre la incidencia y la gravedad de los síntomas de abstinencia en relación con la duración del tratamiento y la dosis de pregabalina.
04.9 Sobredosis
Con sobredosis de hasta 15 g, no se han notificado reacciones adversas inesperadas.
Durante el período de poscomercialización, las reacciones adversas observadas con mayor frecuencia cuando se tomó pregabalina en dosis superiores a las recomendadas incluyeron somnolencia, confusión, agitación e inquietud.
El tratamiento de la sobredosis de pregabalina debe incluir medidas de soporte generales y, si es necesario, puede incluir hemodiálisis (ver sección 4.2 Tabla 1).
05.0 PROPIEDADES FARMACOLÓGICAS
05.1 Propiedades farmacodinámicas
Grupo farmacoterapéutico: Antiepilépticos, otros antiepilépticos.
Código ATC: N03AX16
El principio activo, la pregabalina, es un análogo (ácido (S-3- (aminometil) -5-metilhexanoico) del ácido gamma-aminobutírico.
Mecanismo de acción
La pregabalina se une a la subunidad accesoria (proteína α2-δ) de los canales de calcio dependientes de voltaje en el sistema nervioso central.
Experiencia clínica
Dolor neuropático
La eficacia se ha demostrado en ensayos en neuropatía diabética, neuralgia postherpética y lesión de la médula espinal, pero no se ha estudiado en otros modelos de dolor neuropático.
La pregabalina se ha estudiado en 10 ensayos clínicos controlados, en los que se administró dos veces al día (BID) durante hasta 13 semanas y 3 veces al día (TID) durante hasta 8 semanas. En general, los perfiles de seguridad y eficacia de los regímenes de dosificación BID y TID fueron similares.
En ensayos clínicos de hasta 12 semanas en el dolor neuropático central y periférico se observó una reducción del dolor después de una semana de tratamiento y esta reducción se mantuvo durante la duración del tratamiento.
En ensayos clínicos controlados sobre dolor neuropático periférico, el 35% de los pacientes tratados con pregabalina y el 18% de los pacientes tratados con placebo informaron una mejora del 50% en la puntuación del dolor. En los pacientes que no informaron somnolencia, esta mejora se observó en el 33% de los pacientes tratados con pregabalina y en el 18% de los pacientes tratados con placebo. La tasa de respuesta para los pacientes que informaron somnolencia fue del 48% para los pacientes tratados con pregabalina y del 16% para los pacientes tratados con placebo.
En el ensayo clínico controlado en el dolor neuropático central, el 22% de los pacientes tratados con pregabalina y el 7% de los que tomaron placebo informaron una mejora del 50% en la puntuación del dolor.
Epilepsia
Tratamiento adicional
La pregabalina se ha estudiado en 3 ensayos clínicos controlados de 12 semanas con dos (BID) y tres (TID) administraciones diarias. En general, los perfiles de seguridad y eficacia para los regímenes de dosificación BID o TID fueron similares.
Se observó una reducción en la frecuencia de las convulsiones dentro de una semana de tratamiento.
Monoterapia (pacientes recién diagnosticados)
La pregabalina se estudió en un ensayo clínico controlado que duró 56 semanas con dos dosis diarias (BID). La pregabalina no mostró no inferioridad a la lamotrigina y consideró como criterio de valoración un período de 6 meses sin convulsiones. La pregabalina y la lamotrigina fueron igualmente seguras y bien toleradas.
Trastorno de ansiedad generalizada
La pregabalina se estudió en 6 ensayos clínicos controlados que duraron de 4 a 6 semanas, un estudio de 8 semanas en sujetos de edad avanzada y una fase de prevención de recaídas doble ciego a largo plazo de 6 meses.
Se observó un "alivio de los síntomas del trastorno de ansiedad generalizada" en la escala de ansiedad de Hamilton (HAM-A) dentro de una semana de tratamiento.
En ensayos clínicos controlados (de 4 a 8 semanas de duración), el 52% de los pacientes tratados con pregabalina y el 38% de los del grupo placebo informaron una mejora de al menos el 50% en la puntuación total de la HAM-A desde el inicio hasta el final del estudio.
En ensayos controlados, se notificó visión borrosa en una mayor proporción de pacientes tratados con pregabalina que en pacientes tratados con placebo y se resolvió en la mayoría de los casos con el tratamiento continuado. Se realizó una prueba oftalmológica (que incluyó prueba de agudeza visual, examen formal del campo visual y examen fundoscópico de pupila dilatada) en más de 3600 pacientes inscritos en ensayos clínicos controlados. En estos pacientes, la agudeza visual se redujo en un 6,5% en los pacientes tratados con pregabalina y en un 4,8%. en pacientes tratados con placebo. Se observaron cambios en el campo visual en el 12,4% de los pacientes que tomaban pregabalina y el 11,7% de los que tomaban placebo, pregabalina y en el 2,1% de los tratados con placebo.
05.2 Propiedades farmacocinéticas
La farmacocinética en estado estacionario de pregabalina es similar en voluntarios sanos, pacientes epilépticos que reciben medicamentos antiepilépticos y pacientes con dolor crónico.
Absorción
La pregabalina se absorbe rápidamente cuando se administra en ayunas, alcanzándose las concentraciones plasmáticas máximas dentro de la hora siguiente a la administración de dosis únicas o múltiples. La biodisponibilidad oral de pregabalina es ≥ 90% y es independiente de la dosis. Después de la administración repetida, el estado de equilibrio se alcanza en 24-48 horas. La tasa de absorción de pregabalina disminuye cuando se administra con alimentos, con una reducción de la Cmax de aproximadamente un 25-30% y un retraso de la t de aproximadamente 2,5 horas. Sin embargo, la administración de pregabalina con alimentos no tiene un efecto clínicamente significativo sobre la absorción de pregabalina.
Distribución
En estudios preclínicos, se ha demostrado que la pregabalina atraviesa la barrera hematoencefálica en ratones, ratas y monos. Se ha demostrado que la pregabalina atraviesa la placenta en ratas y está presente en la leche de ratas lactantes. En humanos, el volumen aparente de distribución de pregabalina tras la administración oral es de aproximadamente 0,56 l / kg. La pregabalina no se une a las proteínas plasmáticas.
Biotransformación
La pregabalina se metaboliza de forma insignificante en los seres humanos. Tras la administración de una dosis de pregabalina marcada radiactivamente, aproximadamente el 98% de la radiactividad encontrada en la orina estaba presente como fármaco inalterado. El derivado N-metilado de la pregabalina, el principal metabolito de la pregabalina que se encuentra en la orina, corresponde a 0,9% de la dosis En estudios preclínicos, no hubo indicios de racemización del enantiómero S pregabalina a enantiómero R.
Eliminación
La pregabalina se elimina de la circulación principalmente por excreción renal en forma de fármaco inalterado. La semivida de eliminación media de pregabalina es de 6,3 horas. El aclaramiento plasmático y renal son directamente proporcionales al aclaramiento de creatinina (ver sección 4.2 Insuficiencia renal).
Se requiere un ajuste de dosis en pacientes con insuficiencia renal o sometidos a hemodiálisis (ver sección 4.2 Tabla 1).
Linealidad / no linealidad
La farmacocinética de pregabalina es lineal en el rango de dosis diaria recomendada. La variabilidad entre sujetos en la farmacocinética es baja (
Farmacocinética en grupos particulares de pacientes.
Sexo
Los estudios clínicos indican que el sexo no afecta significativamente las concentraciones plasmáticas de pregabalina.
Insuficiencia renal
El aclaramiento de pregabalina es directamente proporcional al aclaramiento de creatinina. Además, la pregabalina se elimina eficazmente del plasma mediante hemodiálisis (después de una sesión de hemodiálisis de 4 horas, las concentraciones plasmáticas de pregabalina se reducen en aproximadamente un 50%). Dado que la eliminación renal es la vía principal de eliminación, se requiere una reducción de la dosis en pacientes con insuficiencia renal y se requiere una dosis adicional después de una sesión de hemodiliasis (ver sección 4.2 Tabla 1).
Deterioro hepático
No se han realizado estudios farmacocinéticos específicos en pacientes con insuficiencia hepática. Dado que la pregabalina no se metaboliza significativamente y se excreta principalmente como fármaco inalterado en la orina, no se espera que la insuficiencia hepática altere significativamente las concentraciones plasmáticas de pregabalina.
Ancianos (mayores de 65 años)
El aclaramiento de pregabalina tiende a disminuir con la edad. Esta disminución del aclaramiento de la pregabalina administrada por vía oral es coherente con la disminución del aclaramiento de creatinina asociada con el aumento de la edad. Puede ser necesaria una reducción de la dosis de pregabalina en pacientes con insuficiencia renal relacionada con la edad (ver sección 4.2 Tabla 1).
05.3 Datos preclínicos sobre seguridad
En base a los estudios de farmacología de seguridad en animales convencionales, la pregabalina fue bien tolerada a dosis clínicamente significativas. En estudios de toxicidad a dosis repetidas en ratas y monos, se observaron efectos sobre el SNC que incluyen hipoactividad, hiperactividad y ataxia. Se observó comúnmente una mayor incidencia de atrofia retiniana en ancianos. rata albina después de una exposición prolongada a pregabalina con una exposición ≥ 5 veces la exposición humana media a las dosis clínicas máximas recomendadas.
La pregabalina no fue teratogénica en ratones, ratas o conejos. La toxicidad fetal ocurrió en ratas y conejos solo con exposiciones suficientemente superiores a la exposición humana. En los estudios de toxicidad prenatal / posnatal, la pregabalina indujo toxicidad en el desarrollo en ratas con una exposición> 2 veces la exposición humana máxima recomendada.
Los efectos adversos sobre la fertilidad en ratas macho y hembra se observaron solo con exposiciones suficientemente superiores a la exposición terapéutica. Los efectos adversos en los órganos reproductores y los parámetros del esperma de ratas macho son reversibles y solo ocurren en un momento. Exposición por encima de la terapéutica o están asociados con un proceso degenerativo espontáneo del órgano reproductor de la rata macho. Sin embargo, los efectos se consideran menores o, en cualquier caso, no tienen relevancia clínica.
La pregabalina no demostró ser genotóxica según los resultados de una serie de pruebas. in vitro y en vivo.
Se realizaron estudios de carcinogenicidad de dos años con pregabalina en ratas y ratones. No se observó formación de tumores en ratas expuestas a dosis de hasta 24 veces la exposición media en humanos a la dosis clínica máxima recomendada de 600 mg / día. En ratones, no se observó una mayor incidencia de tumores con exposiciones similares a la exposición media en humanos, pero se observó una mayor incidencia de hemangiosarcoma con exposiciones más altas. El mecanismo no genotóxico de la formación de tumores inducida por pregabalina en ratones causa cambios plaquetarios y la proliferación de células endoteliales asociada.Estos cambios plaquetarios no se han encontrado en ratas ni en humanos según los datos clínicos limitados a corto y largo plazo. No hay evidencia que sugiera un riesgo asociado en humanos.
En ratas jóvenes, los tipos de toxicidad no difirieron cualitativamente de los observados en ratas adultas. Sin embargo, las ratas jóvenes son más sensibles. En exposiciones terapéuticas, hubo signos clínicos de hiperactividad y bruxismo en el SNC y algunos cambios en el crecimiento (reducción transitoria del aumento de peso). Se observaron efectos sobre el ciclo menstrual con 5 veces la exposición terapéutica en "Humanos. Una reducción en la respuesta a los estímulos acústicos se observó en ratas jóvenes 1-2 semanas después de una exposición 2 veces mayor que la exposición terapéutica humana. Nueve semanas después de la exposición, este efecto ya no se observó.
06.0 INFORMACIÓN FARMACÉUTICA
06.1 Excipientes
Contenido de la cápsula:
Lactosa monohidrato
Maicena
Talco
Opérculo de la cápsula:
Gelatina
Dióxido de titanio (E171)
Lauril Sulfato de Sodio
Sílice coloidal anhidra
Agua purificada
Óxido de hierro rojo (E172)
Tinta:
Goma laca
Óxido de hierro negro (E172)
Propilenglicol
Hidróxido de potasio
06.2 Incompatibilidad
Irrelevante.
06.3 Período de validez
3 años.
06.4 Precauciones especiales de conservación
Este medicamento no requiere condiciones especiales de conservación.
06.5 Naturaleza del envase primario y contenido del envase.
Blísteres de PVC / Aluminio que contienen 21, 84 o 100 cápsulas duras.
100 x 1 cápsulas duras en blísters unidosis perforados de PVC / Aluminio.
Es posible que no se comercialicen todos los tamaños de envases.
06.6 Instrucciones de uso y manipulación
No hay instrucciones especiales para su eliminación.
07.0 TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
Pfizer Limited,
Ramsgate Road,
Emparedado,
Kent - CT13 9NJ
Reino Unido
08.0 NÚMERO DE AUTORIZACIÓN DE COMERCIALIZACIÓN
EU / 1/04/279/014 - AIC n. 036476149
EU / 1/04/279/015 - AIC n. 036476152
EU / 1/04/279/016 - AIC n. 036476164
EU / 1/04/279/39
09.0 FECHA DE LA PRIMERA AUTORIZACIÓN O RENOVACIÓN DE LA AUTORIZACIÓN
Fecha de la primera autorización: 6 de julio de 2004
Fecha de la última renovación: 06 de julio de 2009
10.0 FECHA DE REVISIÓN DEL TEXTO
11/2011