Ingredientes activos: Denosumab
XGEVA 120 mg solución inyectable.
Indicaciones ¿Por qué se usa Xgeva? ¿Para qué sirve?
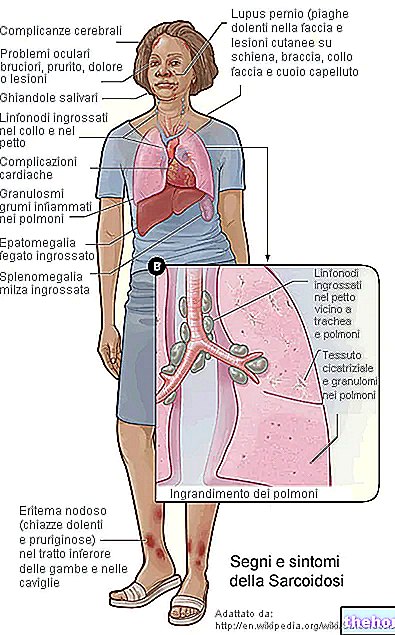
XGEVA contiene denosumab, una proteína (anticuerpo monoclonal) que actúa para disminuir la destrucción ósea causada por el cáncer que se disemina al hueso (metástasis óseas) o el cáncer de hueso de células gigantes.
XGEVA se usa en adultos con cáncer para prevenir complicaciones graves causadas por metástasis óseas (p. Ej., Fractura, presión sobre la médula ósea o la necesidad de radioterapia o cirugía). XGEVA también se utiliza para tratar el cáncer de hueso de células gigantes, que no se puede tratar con cirugía o cuando la cirugía no es la mejor opción, en adultos y adolescentes cuyos huesos han dejado de crecer.
Contraindicaciones Cuándo no se debe usar Xgeva
No use XGEVA
- si es alérgico al denosumab oa cualquiera de los demás componentes de XGEVA.
Su profesional sanitario no le administrará XGEVA si tiene un nivel muy bajo de calcio en sangre que no ha sido tratado.
Su profesional de la salud no le administrará XGEVA si tiene alguna herida que no haya sanado de una cirugía dental u oral.
Precauciones de uso Lo que necesita saber antes de tomar Xgeva
Suplemento de calcio y vitamina D
Debe tomar suplementos de calcio y vitamina D mientras esté en tratamiento con XGEVA, a menos que sus niveles de calcio en sangre sean altos. Su médico discutirá esto con usted. Si su nivel de calcio en sangre es bajo, su médico puede decidir darle suplementos de calcio antes de comenzar el tratamiento con XGEVA.
Niveles bajos de calcio en sangre.
Informe a su médico de inmediato si experimenta espasmos musculares, espasmos o calambres y / o entumecimiento u hormigueo en los dedos de las manos y los pies o alrededor de la boca y / o convulsiones, confusión o pérdida del conocimiento mientras toma XGEVA. Puede tener niveles bajos de calcio en sangre.
Informe a su médico si tiene o alguna vez ha padecido problemas renales graves, insuficiencia renal o si se ha sometido a diálisis, ya que puede aumentar el riesgo de tener niveles bajos de calcio en sangre, especialmente si no toma suplementos de calcio.
Problemas con la boca, los dientes o la mandíbula.
Se ha notificado con frecuencia un efecto secundario llamado osteonecrosis de la mandíbula (degeneración ósea grave de la mandíbula) (puede afectar hasta 1 de cada 10 personas) en pacientes que reciben inyecciones de XGEVA para enfermedades relacionadas con el cáncer.
La osteonecrosis de la mandíbula también puede ocurrir después de suspender el tratamiento.
Es importante tratar de prevenir el desarrollo de osteonecrosis de la mandíbula, ya que es una condición dolorosa que puede ser difícil de tratar. Para reducir el riesgo de desarrollar osteonecrosis de la mandíbula es necesario tomar ciertas precauciones.
Antes de recibir tratamiento, informe a su médico / enfermero (profesional de la salud) si tiene algún problema con la boca o los dientes. Su médico debe retrasar el inicio del tratamiento si tiene heridas en la boca que no han cicatrizado por procedimientos dentales o cirugía oral. Su médico puede pedirle que se someta a un examen dental antes de comenzar el tratamiento con XGEVA.
Durante el tratamiento es necesario mantener una buena higiene bucal y someterse a revisiones dentales periódicas. Si usa prótesis, debe asegurarse de que estén insertadas correctamente.
Si está en tratamiento dental o planea someterse a una cirugía dental (por ejemplo, extracciones dentales), informe a su médico de tratamiento dental e informe a su dentista que está siendo tratado con XGEVA.
Comuníquese con su médico y dentista de inmediato si nota algún problema con la boca o los dientes, como balanceo de los dientes, dolor o hinchazón, o si las llagas o secreciones en la boca no cicatrizan, ya que podrían ser signos de osteonecrosis de la mandíbula / maxilar. .
Los pacientes sometidos a quimioterapia y / o radioterapia, que toman esteroides o medicamentos antiangiogénicos (utilizados para tratar el cáncer), que se someten a una cirugía dental, que no reciben atención dental de rutina o que padecen encías, son fumadores, pueden tener un mayor riesgo de desarrollar osteonecrosis de la mandíbula. .
Fracturas inusuales del fémur
Algunas personas han desarrollado fracturas inusuales en el fémur durante el tratamiento con XGEVA. Comuníquese con su médico si experimenta un dolor nuevo o inusual en la cadera, la ingle o el muslo.
Niños y adolescentes
XGEVA no está recomendado para niños y adolescentes menores de 18 años, excepto para adolescentes con tumor óseo de células gigantes cuyos huesos han dejado de crecer No se ha estudiado el uso de XGEVA en niños y adolescentes con otros tumores que han invadido el hueso.
Interacciones ¿Qué medicamentos o alimentos pueden cambiar el efecto de Xgeva?
Informe a su médico o farmacéutico si está tomando, ha tomado recientemente o podría tomar cualquier otro medicamento, incluso los adquiridos sin receta. En particular, es importante que informe a su médico si está tomando
- otro medicamento que contenga denosumab
- un bisfosfonato.
No debe tomar XGEVA junto con otros medicamentos que contengan denosumab o bisfosfonatos.
Advertencias Es importante saber que:
Embarazo y lactancia
XGEVA no se ha estudiado en mujeres embarazadas. Es importante que informe a su médico si está embarazada, sospecha o planea quedar embarazada. No se recomienda el uso de XGEVA si está embarazada. Las mujeres en edad fértil deben utilizar un método anticonceptivo eficaz mientras toman XGEVA y durante al menos 5 meses después de suspender el tratamiento con XGEVA.
Si queda embarazada durante el tratamiento con XGEVA o menos de 5 meses después de interrumpir el tratamiento con XGEVA, informe a su médico. Se le anima a inscribirse en el Programa de Vigilancia del Embarazo de Amgen. Los detalles del representante local de Amgen se proporcionan en la sección 6 de este prospecto.
No se sabe si XGEVA se excreta en la leche materna. Es importante que informe a su médico si está amamantando o planea hacerlo. A continuación, su médico le ayudará a decidir si debe interrumpir la lactancia o dejar de tomar XGEVA, teniendo en cuenta el beneficio de la lactancia para el niño y el beneficio de tomar XGEVA para la madre.
Si está en periodo de lactancia mientras toma XGEVA, informe a su médico. Se la anima a inscribirse en el Programa de vigilancia de la lactancia de Amgen.Los detalles del representante local de Amgen se proporcionan en la sección 6 de este prospecto.
Consulte a su médico o farmacéutico antes de usar este medicamento.
Conducción y uso de máquinas
La influencia de XGEVA sobre la capacidad para conducir o utilizar máquinas es nula o insignificante.
XGEVA contiene sorbitol
Si su médico le ha dicho que tiene una "intolerancia a algunos azúcares, consulte con él antes de tomar este medicamento, ya que contiene sorbitol (E420)".
XGEVA contiene sodio
Este medicamento contiene menos de 1 mmol de sodio (23 mg) por 120 mg, es decir, esencialmente "exento de sodio".
Dosis, método y momento de administración Cómo usar Xgeva: Posología
La dosis recomendada de XGEVA es de 120 mg administrados una vez cada 4 semanas, como una sola inyección debajo de la piel (subcutánea). XGEVA se inyectará en el muslo, el abdomen o la parte superior del brazo. Si está en tratamiento por cáncer de hueso de células gigantes, recibirá una dosis adicional 1 semana y 2 semanas después de la primera dosis.
XGEVA debe administrarse bajo la responsabilidad de un profesional sanitario.
No agite excesivamente.
También debe tomar suplementos de calcio y vitamina D mientras esté en tratamiento con XGEVA. Su médico discutirá esto con usted.
Si tiene cualquier otra duda sobre el uso de este medicamento, consulte a su médico, farmacéutico o enfermero.
Efectos secundarios ¿Cuáles son los efectos secundarios de Xgeva?
Como todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Informe a su médico de inmediato si nota alguno de estos síntomas mientras toma XGEVA:
- espasmos, espasmos, calambres musculares, entumecimiento u hormigueo en los dedos de las manos y los pies o alrededor de la boca y / o convulsiones, confusión o pérdida del conocimiento. Estos signos pueden indicar niveles bajos de calcio en sangre. Los niveles bajos de calcio en sangre también pueden provocar un cambio en el ritmo cardíaco llamado prolongación del intervalo QT, que se observa en la electrocardiografía (ECG).
Informe a su médico y dentista de inmediato si experimenta alguno de estos síntomas durante el tratamiento con XGEVA o después de interrumpir el tratamiento con XGEVA:
- dolor en la boca y / o mandíbula, hinchazón o llagas que no cicatrizan en la boca o mandíbula, secreción, entumecimiento o sensación de pesadez en la mandíbula, o bamboleo de un diente, ya que estos signos podrían indicar una degeneración ósea grave de la mandíbula ( osteonecrosis).
Efectos adversos muy frecuentes (pueden afectar a más de 1 de cada 10 personas):
- dolor en los huesos, articulaciones y / o músculos a veces intenso,
- sibilancias (disnea),
- Diarrea.
Efectos adversos frecuentes (pueden afectar hasta 1 de cada 10 personas):
- niveles bajos de calcio en sangre (hipocalcemia),
- niveles bajos de fosfato en sangre (hipofosfatemia),
- dolor persistente y / o llagas que no cicatrizan en la boca o en la mandíbula (osteonecrosis de la mandíbula),
- extracción dental,
- sudoración excesiva.
Efectos adversos raros (pueden afectar hasta 1 de cada 1.000 personas):
- reacciones alérgicas (p. ej., sibilancias o dificultad para respirar; hinchazón de la cara, labios, lengua, garganta u otras partes del cuerpo; erupción, picor o urticaria en la piel). En casos raros, las reacciones alérgicas pueden ser graves.
- un dolor nuevo o inusual en la cadera, la ingle o el muslo (esto podría ser un signo temprano de una posible fractura del fémur).
Notificación de efectos secundarios
Si experimenta algún efecto adverso, hable con su médico o enfermero. Esto incluye cualquier posible efecto adverso que no se mencione en este prospecto. También puede notificar los efectos secundarios directamente a través del sistema nacional de notificación incluido en el Apéndice V. Al notificar efectos secundarios, puede ayudar proporcionar más información sobre la seguridad de este medicamento.
Caducidad y retención
Mantenga este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en la etiqueta y la caja después de CAD. La fecha de caducidad se refiere al último día de ese mes.
Conservar en nevera (entre 2 ° C y 8 ° C).
No congelar.
Conservar en el paquete original para proteger el medicamento de la luz.
El vial se puede dejar fuera de la nevera para que alcance la temperatura ambiente (hasta 25 ° C) antes de la inyección, lo que hará que la inyección sea más cómoda. Una vez que el vial haya alcanzado la temperatura ambiente (hasta 25 ° C), debe usarse dentro de los 30 días.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que no necesita, ya que esto ayudará a proteger el medio ambiente.
Fecha límite "> Otra información
Que contiene XGEVA
- El ingrediente activo es denosumab. Cada vial contiene 120 mg en 1,7 ml de solución (correspondiente a 70 mg / ml).
- Los demás componentes son ácido acético glacial, hidróxido de sodio, sorbitol (E420) y agua para preparaciones inyectables.
Descripción del aspecto de XGEVA y contenido del envase
XGEVA es una solución inyectable en un vial.
Cada paquete contiene uno, tres o cuatro viales.
Es posible que no se comercialicen todos los tamaños de envases.
XGEVA es una solución transparente, de incolora a ligeramente amarilla. Puede contener trazas de partículas claras a blancas.
Prospecto fuente: AIFA (Agencia Italiana de Medicamentos). Contenido publicado en enero de 2016. Es posible que la información presente no esté actualizada.
Para tener acceso a la versión más actualizada, es recomendable acceder al sitio web de la AIFA (Agencia Italiana de Medicamentos). Descargo de responsabilidad e información útil.
01.0 NOMBRE DEL MEDICAMENTO -
SOLUCIÓN PARA INYECCIÓN XGEVA 120 MG
▼ Medicamento sujeto a seguimiento adicional. Esto permitirá la identificación rápida de nueva información de seguridad. Se invita a los profesionales sanitarios a notificar cualquier sospecha de reacciones adversas. Consulte la sección 4.8 para obtener información sobre cómo notificar las reacciones adversas.
02.0 COMPOSICIÓN CUALITATIVA Y CUANTITATIVA -
Cada vial contiene 120 mg de denosumab en 1,7 ml de solución (70 mg / ml).
El denosumab es un anticuerpo monoclonal de tipo IgG2 humano producido en una línea de células de mamífero (CHO) mediante tecnología de ADN recombinante.
Excipiente (s) con efecto conocido
Cada 1,7 ml de solución contiene 78 mg de sorbitol (E420).
Para consultar la lista completa de excipientes, ver sección 6.1.
03.0 FORMA FARMACÉUTICA -
Solución inyectable (inyectable).
Solución transparente, de incolora a ligeramente amarilla que puede contener trazas de partículas de proteína translúcidas a blancas.
04.0 INFORMACIÓN CLÍNICA -
04.1 Indicaciones terapéuticas -
Prevención de eventos relacionados con el esqueleto (fracturas patológicas, radioterapia ósea, compresión de la médula espinal o cirugía ósea) en adultos con metástasis óseas de tumores sólidos.
Tratamiento de adultos y adolescentes esqueléticamente maduros con tumor óseo de células gigantes irresecable o en quienes la resección quirúrgica podría causar una morbilidad grave.
04.2 Posología y forma de administración -
XGEVA debe administrarse bajo la responsabilidad de un profesional sanitario.
Dosis
Se requiere la suplementación de al menos 500 mg de calcio y 400 UI de vitamina D al día en todos los pacientes excepto en la hipercalcemia (ver sección 4.4).
Los pacientes en tratamiento con XGEVA deben recibir el prospecto y la tarjeta recordatorio para el paciente.
Prevención de eventos relacionados con el esqueleto en adultos con metástasis óseas de tumores sólidos
La dosis recomendada es de 120 mg administrados en una única inyección subcutánea una vez cada 4 semanas en el muslo, el abdomen o la parte superior del brazo.
Tumor de células gigantes de hueso
La dosis recomendada de XGEVA es de 120 mg, administrada en una única inyección subcutánea, una vez cada 4 semanas en el muslo, abdomen o parte superior del brazo, con dosis adicionales de 120 mg los días 8 y 15 de tratamiento en el primer mes de tratamiento.
Los pacientes del estudio de fase II que se sometieron a una resección completa de un tumor óseo de células gigantes recibieron un tratamiento adicional de 6 meses después de la cirugía según el protocolo del estudio.
Los pacientes con cáncer de hueso de células gigantes deben ser evaluados a intervalos regulares para determinar si continúan beneficiándose del tratamiento. En pacientes cuya enfermedad está controlada por XGEVA, no se ha evaluado el efecto de suspender o suspender el tratamiento; sin embargo, los datos de estos estudios son limitados. los pacientes no indican un efecto rebote al suspender el tratamiento.
Pacientes con insuficiencia renal
No es necesario un ajuste de dosis en pacientes con insuficiencia renal (ver secciones 4.4 para recomendaciones sobre la monitorización de los niveles de calcio, 4.8 y 5.2).
Pacientes con insuficiencia hepática
No se ha estudiado la seguridad y eficacia de denosumab en pacientes con insuficiencia hepática (ver sección 5.2).
Pacientes de edad avanzada (edad ≥ 65 años)
No se requiere ajuste de dosis en pacientes de edad avanzada (ver sección 5.2).
Población pediátrica
No se ha establecido la seguridad y eficacia de XGEVA en pacientes pediátricos (edad
XGEVA no se recomienda en pacientes pediátricos (edad
Tratamiento de adolescentes esqueléticamente maduros con tumor óseo de células gigantes irresecable o en quienes la resección quirúrgica podría causar morbilidad grave: la posología es la misma que para los adultos.
En estudios con animales, la inhibición del ligando RANK / RANK (RANKL) se ha asociado con la inhibición del crecimiento óseo y la falta de erupción y estos cambios fueron parcialmente reversibles después de la interrupción de la inhibición de RANKL (ver párrafo 5.3).
Método de administración
Para uso subcutáneo.
Para obtener instrucciones de uso, manipulación y eliminación, consulte la sección 6.6.
04.3 Contraindicaciones -
Hipersensibilidad al principio activo oa alguno de los excipientes incluidos en la sección 6.1.
Hipocalcemia grave no tratada (ver sección 4.4).
Lesiones que no se curan con cirugía dental u oral.
04.4 Advertencias especiales y precauciones de uso apropiadas -
Suplemento de calcio y vitamina D
Es importante que todos los pacientes reciban una ingesta adecuada de calcio y vitamina D, excepto en caso de hipercalcemia (ver sección 4.2).
Hipocalcemia
La hipocalcemia preexistente debe corregirse antes de iniciar el tratamiento con XGEVA.
La hipocalcemia puede ocurrir en cualquier momento durante el tratamiento con XGEVA. El control de los niveles de calcio debe realizarse antes de la dosis inicial de XGEVA, dentro de las dos semanas posteriores a la dosis inicial, en caso de sospecha de síntomas de hipocalcemia (ver la lista de síntomas en la sección 4.8). . Se debe considerar la monitorización adicional de los niveles de calcio durante el tratamiento en pacientes con factores de riesgo de hipocalcemia, o según se indique de otro modo en función del estado clínico del paciente.
Se debe animar a los pacientes a que informen de los síntomas indicativos de hipocalcemia. Si se desarrolla hipocalcemia durante la administración de XGEVA, se requieren suplementos de calcio adicionales y monitorización adicional.
Durante el uso poscomercialización, se han notificado casos de hipocalcemia sintomática grave (incluidos casos mortales) (ver sección 4.8), y la mayoría de los casos se producen en las primeras semanas tras el inicio del tratamiento, pero pueden aparecer más tarde.
Insuficiencia renal
Los pacientes con insuficiencia renal grave (diálisis con aclaramiento de creatinina tienen un mayor riesgo de desarrollar hipocalcemia. El riesgo de desarrollar hipocalcemia y las consiguientes elevaciones de los niveles de hormona paratiroidea aumentan con el grado de insuficiencia renal. Monitoreo regular de los niveles de enfermedad renal. El calcio es especialmente importante en estos pacientes.
Osteonecrosis de la mandíbula (ONJ)
Se ha notificado con frecuencia ONM en pacientes que reciben XGEVA (ver sección 4.8).
El inicio del tratamiento / un nuevo tratamiento debe posponerse en pacientes con lesiones de tejidos blandos abiertos y sin cicatrizar en la boca. Se recomienda un examen dental con profilaxis dental y una evaluación individual del beneficio / riesgo antes del tratamiento con XGEVA.
Se deben considerar los siguientes factores de riesgo al evaluar el riesgo de un paciente de desarrollar ONM:
• la potencia del fármaco que inhibe la resorción ósea (el riesgo es mayor con fármacos más potentes), la vía de administración (el riesgo es mayor con la administración parenteral) y la dosis acumulativa de la terapia de resorción ósea.
• tumor, enfermedades comórbidas (p. Ej. Anemia, coagulopatías, infección), tabaquismo.
• terapias concomitantes: corticosteroides, quimioterapia, inhibidores de la angiogénesis, radioterapia de la región de la cabeza y el cuello.
• mala higiene bucal, enfermedad periodontal, prótesis dentales insertadas incorrectamente, enfermedad dental preexistente, procedimientos dentales invasivos (por ejemplo, extracciones dentales).
Se debe alentar a todos los pacientes a que mantengan una buena higiene bucal, se sometan a revisiones dentales periódicas e informen inmediatamente de cualquier síntoma bucal, como movilidad de los dientes, dolor o hinchazón, llagas bucales que no cicatrizan o presencia de secreciones durante el tratamiento. . Durante el tratamiento, los procedimientos dentales invasivos solo deben realizarse después de una cuidadosa consideración y deben evitarse en las proximidades de la administración de XGEVA.
El tratamiento de los pacientes que desarrollan ONM debe realizarse en estrecha colaboración entre el médico tratante y un dentista o cirujano maxilofacial con experiencia en el tratamiento de ONM. Se debe considerar la interrupción temporal del tratamiento con XGEVA hasta que se resuelva la afección y, cuando sea posible, para mitigar los factores de riesgo que contribuyeron a su aparición.
Fracturas atípicas del fémur.
Se han notificado casos de fracturas atípicas de fémur en pacientes tratados con XGEVA (ver sección 4.8). Las fracturas femorales atípicas pueden ocurrir con un traumatismo mínimo o nulo en las regiones subtrocantérea y diafisaria del fémur. Estos eventos se caracterizan por hallazgos radiográficos específicos. También se han notificado fracturas atípicas de fémur en pacientes con algunas enfermedades concomitantes (p. Ej., Deficiencia de vitamina D, artritis reumatoide, hipofosfatasia) y en el uso de ciertos medicamentos (p. Ej., Bisfosfonatos, glucocorticoides, inhibidores de la bomba de protones). Estos eventos también ocurrieron en ausencia de terapia antirresortiva. Fracturas similares, notificadas en asociación con el uso de bisfosfonatos, a menudo son bilaterales; por lo tanto, el fémur contralateral debe evaluarse en pacientes tratados con denosumab que han sufrido una fractura de la diáfisis femoral. En pacientes con sospecha de fractura femoral atípica, se debe considerar la interrupción del tratamiento con XGEVA, pendiente de la evaluación del paciente basada en un análisis de beneficio / riesgo individual Durante el tratamiento con XGEVA, se debe advertir a los pacientes que informen sobre un dolor nuevo o inusual en el muslo, la cadera o la ingle. Los pacientes que presenten estos síntomas deben ser evaluados en busca de una fractura femoral incompleta.
Pacientes con un sistema esquelético en crecimiento
No se recomienda XGEVA en pacientes con sistemas esqueléticos en crecimiento (ver sección 4.2). Se ha notificado hipercalcemia clínicamente significativa en pacientes con sistemas esqueléticos en crecimiento tratados con XGEVA después de semanas o meses de interrumpir el tratamiento.
Otros
Los pacientes que están siendo tratados con XGEVA no deben ser tratados concomitantemente con otros medicamentos que contengan denosumab (para indicaciones de osteoporosis).
Los pacientes que están en tratamiento con XGEVA no deben recibir tratamiento concomitante con bisfosfonatos.
La degeneración ósea por tumor de células gigantes a enfermedad maligna o la progresión metastásica de la enfermedad son eventos poco frecuentes y representan un riesgo conocido en pacientes con tumor óseo de células gigantes. Los pacientes deben ser monitoreados para detectar signos radiológicos de malignidad, nueva radiolucidez u osteólisis. Los datos clínicos disponibles no sugieren un aumento del riesgo de malignidad en pacientes con tumor óseo de células gigantes tratados con XGEVA.
Advertencias para excipientes
XGEVA contiene sorbitol. Los pacientes con enfermedades hereditarias raras de intolerancia a la fructosa no deben tomar XGEVA.
Este medicamento contiene menos de 1 mmol de sodio (23 mg) por 120 mg, es decir, esencialmente "exento de sodio".
04.5 Interacciones con otros medicamentos y otras formas de interacción -
No se han realizado estudios de interacción.
En estudios clínicos, XGEVA se administró en combinación con tratamientos antitumorales estándar y en pacientes tratados previamente con bisfosfonatos. No hubo alteraciones clínicamente relevantes en la concentración mínima sérica y la farmacodinamia de denosumab (N-telopéptido ajustado a la creatinina urinaria, uNTx / Cr) debido a la terapia hormonal y / o quimioterapia concomitante o la administración intravenosa previa de bisfosfonatos.
04.6 Embarazo y lactancia -
El embarazo
No se dispone de datos adecuados sobre el uso de XGEVA en mujeres embarazadas. La toxicidad para la reproducción se demostró en un estudio en monos cynomolgus con la administración de denosumab durante el embarazo con AUC 12 veces la dosis humana (ver sección 5.3).
No se recomienda el uso de XGEVA en mujeres embarazadas y en mujeres en edad fértil que no estén utilizando anticonceptivos de alta eficacia. Se debe advertir a las mujeres que eviten quedarse embarazadas durante el tratamiento con XGEVA y durante al menos 5 meses después del tratamiento. Tratamiento. Cualquier efecto de Es probable que XGEVA sea mayor durante el segundo y tercer trimestre del embarazo, ya que los anticuerpos monoclonales se transportan a través de la placenta de forma lineal a medida que avanza el embarazo, y la mayor cantidad se transfiere durante el tercer trimestre del embarazo.
Hora de la comida
Se desconoce si denosumab se excreta en la leche materna humana. Los estudios en ratones knockout sugieren que la ausencia de RANKL durante el embarazo podría interferir con la maduración de la glándula mamaria, provocando una alteración de la lactancia después del parto (ver sección 5.3). Se debe tomar una decisión sobre la abstención de la lactancia materna o del tratamiento con XGEVA, teniendo en cuenta el beneficio de la lactancia para el recién nacido / lactante y el beneficio del tratamiento con XGEVA para la mujer.
Fertilidad
No hay datos sobre los efectos del denosumab en la fertilidad humana. Los estudios en animales no indican efectos perjudiciales directos o indirectos sobre la fertilidad (ver sección 5.3).
04.7 Efectos sobre la capacidad para conducir y utilizar máquinas.
La influencia de XGEVA sobre la capacidad para conducir y utilizar máquinas es nula o insignificante.
04.8 Efectos indeseables -
Resumen del perfil de seguridad
El perfil de seguridad general es consistente en todas las indicaciones aprobadas.
La hipocalcemia se notificó con frecuencia después de la administración de XGEVA, principalmente durante las primeras 2 semanas. La hipocalcemia puede ser grave y sintomática (ver sección 4.8 - descripción de reacciones adversas seleccionadas). Las disminuciones en las concentraciones séricas de calcio generalmente se tratan de manera apropiada con suplementos de calcio y vitamina D. Las reacciones adversas más comunes con XGEVA son el dolor musculoesquelético.
La seguridad de XGEVA se ha evaluado en:
• 5.931 pacientes con cánceres avanzados que involucran huesos en ensayos clínicos controlados activos que evalúan la eficacia y seguridad de XGEVA versus ácido zoledrónico en la prevención de eventos relacionados con el esqueleto.
• 523 pacientes con tumor óseo de células gigantes en un ensayo clínico de un solo brazo para evaluar la eficacia y seguridad de XGEVA.
Las reacciones adversas identificadas en estos ensayos clínicos y en el entorno poscomercialización se presentan en la Tabla 1.
Tabla de reacciones adversas
Para la clasificación de reacciones adversas basada en las tasas de incidencia en tres estudios clínicos de fase III y dos de fase II, se utilizó la siguiente convención (ver tabla 1): muy frecuentes (≥ 1/10), frecuentes (≥ 1/100,
Tabla 1: Reacciones adversas notificadas en pacientes con cánceres avanzados que involucran huesos o cáncer de hueso de células gigantes
¹ Ver sección Descripción de reacciones adversas seleccionadas.
² Ver sección Otras poblaciones especiales
Descripción de reacciones adversas seleccionadas
Hipocalcemia
En tres ensayos clínicos de fase III controlados con activos en pacientes con cánceres avanzados que afectaban a los huesos, se notificó hipocalcemia en el 9,6% de los pacientes tratados con XGEVA y en el 5,0% de los pacientes tratados con ácido zoledrónico.
Se detectó una disminución de grado 3 en los niveles de calcio sérico en el 2,5% de los pacientes tratados con XGEVA y en el 1,2% de los pacientes tratados con ácido zoledrónico. Se observó una disminución de grado 4 en los niveles de calcio sérico en el 0,6% de los pacientes tratados con XGEVA y en el 0,2% de los pacientes tratados con XGEVA. de pacientes tratados con ácido zoledrónico (ver sección 4.4).
En dos ensayos clínicos de fase II de un solo brazo en pacientes con tumor óseo de células gigantes, se notificó hipocalcemia en el 5,7% de los pacientes. Ninguno de los eventos adversos se consideró grave.
Durante el uso poscomercialización, se han notificado casos de hipocalcemia sintomática grave (incluidos casos mortales), y la mayoría de los casos se producen en las primeras semanas tras el inicio del tratamiento. Ejemplos de manifestaciones clínicas de hipocalcemia sintomática grave incluyeron prolongación del intervalo QT, tetania, convulsiones y estado mental alterado (incluido coma) (ver sección 4.4). Los síntomas de hipocalcemia en los ensayos clínicos incluyeron parestesia o rigidez muscular, espasmos, espasmos y calambres musculares.
Osteonecrosis de la mandíbula (ONJ)
En los ensayos clínicos, la incidencia de ONM fue mayor con una duración de exposición más prolongada; la ONM también se diagnosticó después del final del tratamiento con XGEVA y la mayoría de los casos ocurrieron dentro de los 5 meses posteriores a la última dosis. Se excluyeron de los ensayos clínicos los pacientes con antecedentes de ONM u osteomielitis de la mandíbula / maxilar, con inflamación activa dentaria o mandibular / maxilar que requiriera cirugía, resultado de una cirugía dental / oral no resuelta, o pacientes para quienes se planificaron procedimientos dentales invasivos.
En las fases de tratamiento primario de tres ensayos clínicos controlados con activo de fase III en pacientes con cánceres avanzados que afectaban al hueso, se confirmó ONM en el 1.8% de los pacientes tratados con XGEVA (mediana de exposición de 12, 0 meses; rango 0.1 - 40.5) y en 1.3 % de pacientes tratados con ácido zoledrónico. Las características clínicas de estos casos fueron similares entre los grupos de tratamiento. Entre los pacientes con ONM confirmada, la mayoría (81% en ambos grupos de tratamiento) tenía antecedentes de extracciones dentales, mala higiene bucal y / o uso de aparatos ortopédicos La mayoría de los sujetos recibieron o habían recibido quimioterapia.
Los estudios clínicos en pacientes con cáncer de mama o de próstata incluyeron una fase de extensión del tratamiento con XGEVA (mediana de exposición general de 14,9 meses; rango de 0,1 a 67,2). La ONM se confirmó en el 6,9% de los pacientes con cáncer de mama y cáncer de próstata durante la fase de extensión del tratamiento.
La incidencia general confirmada de ONM, ajustada por paciente-año, fue del 1,1% durante el primer año de tratamiento, del 3,7% durante el segundo año y del 4,6% en los años posteriores. La mediana de tiempo hasta el inicio de la ONM fue de 20,6 meses (rango: 4-53).
En dos ensayos clínicos de fase II de un solo brazo en pacientes con tumor óseo de células gigantes, la ONM se produjo en el 2,3% (12 de 523) de los pacientes tratados con XGEVA (mediana de exposición global de 20,3 meses; rango: 0-83,4). La incidencia de ONM, ajustada por año paciente, fue del 0,2% durante el primer año de tratamiento y del 1,7% durante el segundo año. La mediana del tiempo hasta el inicio de la ONM fue de 19,4 meses (rango: 11-40). Según la duración de la exposición, no hay datos suficientes para que los pacientes con TCGG evalúen el riesgo de ONM más allá de los 2 años.
En un ensayo clínico de fase III, en pacientes con cáncer de próstata no metastásico (una población de pacientes para la que no está indicado XGEVA), con una "exposición al tratamiento más prolongada (hasta 7 años), la incidencia de ONM confirmada, corregida por paciente- año fue de 1,1% en el primer año de tratamiento, 3,0% en el segundo año y 7,1% en los años siguientes.
Reacciones de hipersensibilidad al fármaco.
Se han notificado casos de hipersensibilidad, incluidas reacciones anafilácticas raras, en pacientes que recibieron XGEVA durante el uso poscomercialización.
Fracturas atípicas del fémur.
En el programa de desarrollo clínico, se han notificado raramente fracturas atípicas de fémur en pacientes tratados con denosumab (ver sección 4.4).
Dolor musculoesquelético
En la fase de poscomercialización, se notificó dolor musculoesquelético, incluidos casos graves, en pacientes tratados con XGEVA. En los ensayos clínicos, el dolor musculoesquelético fue muy común en los grupos de tratamiento con denosumab y ácido zoledrónico. El dolor musculoesquelético que llevó a la interrupción del tratamiento fue poco común.
Población pediátrica
XGEVA se estudió en un estudio clínico abierto en el que participaron 18 adolescentes esqueléticamente maduros con tumor óseo de células gigantes. Con base en estos datos limitados, el perfil de eventos adversos parece ser similar al de los adultos.
Otras poblaciones especiales
Insuficiencia renal
En un ensayo clínico en pacientes con insuficiencia renal grave (aclaramiento de creatinina, suplementación con calcio. El riesgo de desarrollar hipocalcemia durante el tratamiento con XGEVA es mayor a medida que aumenta el grado de insuficiencia renal. En un ensayo clínico en pacientes sin cáncer. En estadio avanzado, 19 % de pacientes con insuficiencia renal grave (aclaramiento de creatinina
También se han observado elevaciones posteriores de los niveles de hormona paratiroidea en pacientes con insuficiencia renal grave o en diálisis tratados con XGEVA. La monitorización de los niveles de calcio y la suplementación adecuada de calcio y vitamina D son particularmente importantes en pacientes con insuficiencia renal (ver sección 4.4).
Notificación de sospechas de reacciones adversas
La notificación de sospechas de reacciones adversas que se produzcan después de la autorización del medicamento es importante, ya que permite un seguimiento continuo de la relación beneficio / riesgo del medicamento. Se solicita a los profesionales sanitarios que notifiquen cualquier sospecha de reacciones adversas a través del sistema nacional de notificación (Agencia Italiana de Medicamentos - Sitio web: http // www.agenziafarmaco.gov.it / it / managers).
04.9 Sobredosis -
No se han notificado casos de sobredosis en estudios clínicos. En los ensayos clínicos, XGEVA se administró en dosis de hasta 180 mg cada 4 semanas y 120 mg por semana durante 3 semanas.
05.0 PROPIEDADES FARMACOLÓGICAS -
05.1 "Propiedades farmacodinámicas -
Grupo farmacoterapéutico: Fármacos para el tratamiento de enfermedades óseas - Otros fármacos que afectan a la estructura y mineralización óseas, código ATC: M05BX04
Mecanismo de acción
RANKL es una proteína y viene en forma transmembrana o soluble. RANKL es esencial para la formación, función y supervivencia de los osteoclastos, el único tipo de célula responsable de la resorción ósea. El aumento de la actividad osteoclástica, estimulado por RANKL, es un mediador clave de la destrucción ósea en la enfermedad ósea metastásica y en el mieloma múltiple. El denosumab es un anticuerpo monoclonal humano (IgG2) que se dirige y se une a RANKL con alta afinidad y especificidad, previniendo la aparición de la interacción RANKL / RANK, reduciendo así el número y función de los osteoclastos, lo que resulta en una disminución de la resorción ósea y destrucción ósea inducida por cáncer. .
Los tumores óseos de células gigantes se caracterizan por células estromales neoplásicas que expresan el ligando RANK y células gigantes similares a los osteoclastos que expresan RANK. En pacientes con cáncer óseo de células gigantes, el denosumab se une al ligando RANK, reduciendo significativamente o eliminando las células similares a los osteoclastos. células gigantes. En consecuencia, la osteólisis se reduce y el estroma proliferativo del tumor se reemplaza por hueso nuevo con una estructura densa, no proliferativa y diferenciada.
Efectos farmacodinámicos
En estudios clínicos de fase II en pacientes con cánceres en estadio avanzado que afectaban a los huesos, la administración subcutánea (sc) de XGEVA cada 4 semanas o cada 12 semanas resultó en una rápida reducción de los marcadores de resorción ósea (uNTx / Cr, Suero CTx), con una mediana de disminución de aproximadamente el 80% para uNTx / Cr dentro de una semana, independientemente de la terapia previa con bisfosfonatos o del nivel de uNTx / Cr inicial. En los estudios clínicos de fase III, se mantuvieron reducciones medias de aproximadamente el 80% en uNTx / Cr después de 3 meses de tratamiento en 2075 pacientes con cáncer avanzado tratados con XGEVA y sin tratamiento previo con bisfosfonatos intravenosos.
Inmunogenicidad
En estudios clínicos, no se observaron anticuerpos neutralizantes dirigidos a XGEVA. Según los resultados de un inmunoensayo sensible, menos del 1% de los pacientes tratados con denosumab durante un máximo de 3 años dieron positivo en anticuerpos no neutralizantes sin evidencia de alteración del perfil de respuesta farmacocinética, toxicológica o clínica.
Eficacia clínica en pacientes con metástasis óseas de tumores sólidos
Eficacia y seguridad de XGEVA 120 mg s.c., administrado cada 4 semanas o ácido zoledrónico 4 mg i.v. (con ajuste de dosis para la función renal reducida), administrados cada 4 semanas, se compararon en tres estudios aleatorizados, doble ciego, controlados con activos en pacientes que no habían recibido tratamiento con bisfosfonatos IV y con cánceres avanzados con afectación ósea: pacientes adultos con cáncer de mama ( estudio 1), otros tumores sólidos o mieloma múltiple (estudio 2) y cáncer de próstata resistente a la castración (estudio 3). dental activo o mandibular / maxilar que requiere cirugía oral, una afección dental / oral no resuelta después de una cirugía, o pacientes programados para cirugía dental invasiva. los procedimientos no fueron elegibles para la inscripción en estos estudios. Los criterios de valoración primarios y secundarios evaluaron la aparición de uno o más eventos relacionados con el esqueleto (SRE). En los estudios que demostraron la superioridad de XGEVA sobre el ácido zoledrónico, se ofreció a los pacientes una fase de extensión. Del tratamiento preespecificado, abierto con XGEVA durante 2 años .
XGEVA redujo el riesgo de desarrollar SRE y de desarrollar SRE múltiples (primero y subsiguientes) en pacientes con metástasis óseas de tumores sólidos (ver Tabla 2).
Tabla 2: Resultados de eficacia en pacientes con cánceres avanzados que afectan a los huesos
NR = no alcanzado; NA = no disponible; MCH = hipercalcemia maligna; SMR = tasa de morbilidad esquelética; HR = índice de riesgo; RRR = reducción del riesgo relativo † Para los estudios 1, 2 y 3, se presentan los valores p ajustados (criterios de valoración: primer SRE y primer SRE y siguientes); * Incluye todos los eventos esqueléticos a lo largo del tiempo; solo se consideran los eventos que ocurrieron ≥ 21 días después del evento anterior.
** Incluyendo NSCLC, cáncer renal, cáncer colorrectal, cáncer de pulmón microcítico, cáncer de vejiga, cáncer de cabeza y cuello, cáncer gastrointestinal / genitourinario y otros cánceres excepto cáncer de mama y próstata
Progresión de la enfermedad y supervivencia general
La progresión de la enfermedad fue similar entre XGEVA y ácido zoledrónico en los tres estudios y en el análisis preespecificado combinado de los tres estudios.
En los tres estudios, la supervivencia global entre XGEVA y ácido zoledrónico se equilibró en pacientes con cánceres avanzados que afectaban a los huesos: pacientes con cáncer de mama (cociente de riesgo e IC del 95%: 0,95 [0,81-1,11]), pacientes con cáncer de próstata (cociente de riesgo y 95% % IC: 1,03 [0,91-1,17]) y pacientes con otros tumores sólidos o mieloma múltiple (índice de riesgo e IC del 95%: 0,95 [0,83-1,08]). En un análisis post-hoc del estudio 2 (pacientes con otros tumores sólidos o mieloma múltiple) se examinó la supervivencia general para los tres tipos de tumores utilizados para la estratificación (cáncer de pulmón de células no pequeñas, mieloma múltiple y más). La supervivencia general fue mayor para XGEVA en el cáncer de pulmón de células no pequeñas (índice de riesgo [IC del 95%] de 0,79 [0,65-0,95]; n = 702), mayor para el ácido zoledrónico en el mieloma múltiple (índice de riesgo [IC del 95%] de 2,26 [1,13- 4,50]; n = 180) y similar para XGEVA y ácido zoledrónico en otros tipos de tumores (cociente de riesgo [IC del 95%] de 1,08 [0,90-1,30]; n = 894). En este estudio no se verificaron factores pronósticos ni tratamientos antineoplásicos. En un análisis preespecificado combinado de los estudios 1, 2 y 3, la supervivencia global fue similar entre XGEVA y ácido zoledrónico (índice de riesgo e IC del 95%: 0,99 [0,91-1,07]).
Efectos sobre el dolor
El tiempo transcurrido hasta la mejora del dolor (es decir, reducción de 2 puntos desde el inicio, en la puntuación de peor dolor de BPI-SF) fue similar para denosumab y ácido zoledrónico en cada estudio y análisis integrado. En un "análisis post-hoc del conjunto de datos combinado, la mediana del tiempo hasta el empeoramiento del dolor (> 4 puntos en la puntuación del dolor de peor intensidad) en pacientes con dolor leve o sin dolor al inicio del estudio se retrasó para XGEVA en comparación con" ácido zoledrónico (198 vs. .143 días) (p = 0,0002).
Eficacia clínica en adultos y adolescentes esqueléticamente maduros con tumor óseo de células gigantes
La seguridad y eficacia de XGEVA se estudiaron en dos ensayos clínicos abiertos de fase II de un solo brazo (estudios 4 y 5) en los que se inscribieron 529 pacientes con tumor óseo de células gigantes irresecable o irresecable. morbosidad.
El estudio 4 incluyó a 37 pacientes adultos con tumor óseo de células gigantes irresecable confirmado histológicamente o tumor óseo de células gigantes recidivante. Los criterios de respuesta incluyeron la eliminación de células gigantes sobre una base histopatológica o la ausencia de progresión sobre una base radiográfica.
De los 35 pacientes incluidos en el análisis de eficacia, el 85,7% (IC del 95%: 69,7-95,2) tuvo una respuesta al tratamiento con XGEVA. Los 20 pacientes (100%) que se sometieron a evaluación histológica respondieron al tratamiento. En los 15 pacientes restantes, 10 (67%) informes radiológicos no mostraron progresión de la lesión diana.
El estudio 5 incluyó a 507 adultos o adolescentes esqueléticamente maduros con tumor óseo de células gigantes y evidencia de enfermedad activa medible.
En la cohorte 1 (pacientes con enfermedad irresecable), no se alcanzó la mediana del tiempo hasta la progresión de la enfermedad, 21 de los 258 pacientes tratados presentaron progresión de la enfermedad. En la cohorte 2 (pacientes con enfermedad resecable, pero para los que la cirugía planificada se asoció con una morbilidad grave), 209 de 228 pacientes evaluables tratados con XGEVA no se sometieron a cirugía en el mes 6. En total, de 225 pacientes para los que fue tumor de células gigantes hueso se programó la cirugía (excluyendo sólo las metástasis pulmonares), 109 no se sometieron a cirugía y 84 se sometieron a procedimientos menos invasivos de lo planeado al inicio del estudio.La mediana de tiempo hasta la cirugía fue de 261 días.
Se realizó una revisión retrospectiva independiente de los datos de imágenes radiológicas en el momento de la inscripción de los 305 pacientes en los Estudios 4 y 5. Ciento noventa tuvieron una respuesta evaluable al menos una vez y se incluyeron en el análisis (Tabla 3). En general, XGEVA logró respuestas objetivas en el 71,6% de los pacientes (IC del 95%: 64,6-77,9) (tabla 3) evaluados mediante diferentes metodologías, y la mayoría de las respuestas se definieron como reducción de la actividad de la PET con fluorodesoxiglucosa o aumento de densidad medido en TC. / HU, solo el 25,1% de los pacientes tuvo una respuesta de acuerdo con RECIST. La mediana del tiempo de respuesta fue de 3,1 meses (IC del 95%: 2,89-3, 65) La duración media de la respuesta no fue evaluable (cuatro pacientes tuvieron progresión de la enfermedad después de la respuesta objetiva. ) En 190 sujetos evaluables para respuesta tumoral objetiva, 55 sujetos con TCGC fueron sometidos a cirugía, 40 de los cuales se sometieron a una resección completa.
Tabla 3: Respuesta objetiva al tratamiento en pacientes con cáncer de hueso de células gigantes
¹ CI = intervalo de confianza exacto
² RECIST 1.1: criterios modificados para evaluar la respuesta en tumores sólidos para evaluar la masa tumoral mediante tomografía axial computarizada (TC) o resonancia magnética (RM).
³ EORTC: criterio modificado de la Organización Europea para la Investigación y el Tratamiento del Cáncer para evaluar la respuesta metabólica mediante el uso de Tomografía por Emisión de Positrones con Fluoruroxiglucosa (FDG-PET).
4Densidad / Tamaño: Criterios de Choi Inverse modificados para evaluar el tamaño y la densidad del tumor utilizando unidades Hounsfield basadas en CT / MRI.
Efecto sobre el dolor
En el momento de la inclusión de 282 pacientes, en el estudio 5, las cohortes 1 y 2 combinadas, se notificó una reducción clínicamente significativa del peor dolor (p. Ej., ≥ 2 puntos de disminución con respecto al valor inicial) en el 31,4% de los pacientes en riesgo (p. Ej., Aquellos que tenían el peor dolor puntuación de ≥ 2 al inicio) dentro de una semana de tratamiento y ≥ 50% en la semana 5. Estas mejoras del dolor se mantuvieron sin cambios en evaluaciones posteriores. El uso inicial de analgésicos antes del tratamiento en la cohorte 1 y la cohorte 2 se evaluó mediante una escala de siete puntos , donde el 74,8% de los pacientes informaron de un uso moderado o no de analgésicos (p. ej., puntuación de analgésicos ≤ 2) y el 25,2% de los pacientes utiliza opioides potentes (p. ej., puntuación de analgésicos de 3 a 7).
Población pediátrica
La Agencia Europea de Medicamentos eximió de la obligación de presentar los resultados de los estudios con XGEVA en todos los subconjuntos de la población pediátrica para la prevención de eventos relacionados con el esqueleto en pacientes con metástasis óseas y en subconjuntos de la población pediátrica menores de 12 años para el tratamiento de Tumor celular óseo (ver sección 4.2 para obtener información sobre uso pediátrico).
En el estudio 5, XGEVA se evaluó en un subgrupo de 18 pacientes adolescentes (de 13 a 17 años) con tumor óseo de células gigantes que habían alcanzado la madurez esquelética definida como al menos un hueso largo maduro (p. Ej., Húmero con crecimiento epifisario cerrado-cerrado del disco placa del húmero) y peso corporal ≥ 45 kg. Se observó una respuesta objetiva en cuatro de seis adolescentes evaluables en un análisis intermedio del estudio 5. Una evaluación de un investigador informó que los 18 pacientes adolescentes tenían la mejor estabilidad o superior respuesta a la enfermedad (respuesta completa en 2 pacientes, respuesta parcial en 8 pacientes y estabilidad de la enfermedad en 8 pacientes). La Agencia Europea de Medicamentos ha retrasado la obligación de presentar los resultados finales de este estudio.
05.2 "Propiedades farmacocinéticas -
Absorción
Tras la administración subcutánea, la biodisponibilidad fue del 62%.
Biotransformación
El denosumab se compone únicamente de aminoácidos y carbohidratos, como las inmunoglobulinas nativas, y es poco probable que se elimine por mecanismos metabólicos hepáticos. Se espera que el metabolismo y la eliminación de los fármacos sigan las vías del aclaramiento de las inmunoglobulinas, es decir, la degradación en pequeños péptidos y aminoácidos individuales.
Eliminación
En sujetos con cáncer avanzado, que recibieron múltiples dosis de 120 mg cada 4 semanas, se observó una acumulación de aproximadamente 2 veces en las concentraciones séricas de denosumab y se alcanzó el estado de equilibrio en 6 meses; esto es consistente con la farmacocinética independiente del tiempo. En sujetos con tumor óseo de células gigantes que recibieron 120 mg cada 4 semanas con una dosis de carga los días 8 y 15, los niveles de estado estacionario se alcanzaron durante el primer mes de tratamiento. Entre las semanas 9 y 49, los niveles medios variaron en menos de 9% En los sujetos que dejaron de tomar 120 mg cada 4 semanas, la semivida media fue de 28 días (rango: 14-55 días).
Un análisis farmacocinético de la población no reveló cambios clínicamente significativos en la exposición sistémica de denosumab en estado estacionario para la edad (18-87 años), raza / grupo étnico (se estudiaron sujetos negros, hispanos, asiáticos y blancos), sexo o tipo de tumor sólido. . El aumento de peso se asoció con reducciones en la exposición sistémica y viceversa. Las alteraciones no se consideraron clínicamente relevantes, ya que los efectos farmacodinámicos basados en los marcadores de recambio óseo fueron constantes en una amplia gama de pesos corporales.
Linealidad / no linealidad
El denosumab exhibió una farmacocinética no lineal a varios niveles de dosis, pero para dosis de 60 mg (o 1 mg / kg) y superiores mostró aumentos de exposición aproximadamente proporcionales a la dosis. La no linealidad se debe probablemente a un mecanismo de eliminación. importante a bajas concentraciones.
Insuficiencia renal
En estudios con denosumab (60 mg, n = 55 y 120 mg, n = 32) en pacientes sin cáncer avanzado pero con diversos grados de función renal, incluidos pacientes en diálisis, el grado de insuficiencia renal no tuvo ningún efecto sobre la farmacocinética de denosumab; por lo tanto, no es necesario ajustar la dosis en caso de insuficiencia renal. No se requiere monitorización renal cuando se recibe XGEVA.
Deterioro hepático
No se han realizado estudios específicos en pacientes con insuficiencia hepática. En general, los anticuerpos monoclonales no se eliminan por metabolismo hepático. Se espera que la farmacocinética del denosumab no se vea afectada por la función hepática alterada.
Personas mayores
En general, no se observaron diferencias en seguridad y eficacia entre pacientes geriátricos y pacientes más jóvenes. Los ensayos clínicos controlados de XGEVA en pacientes mayores de 65 años con neoplasias malignas avanzadas con afectación ósea han demostrado una eficacia y seguridad similares. En sujetos mayores y jóvenes Sin ajuste de dosis se requiere en pacientes de edad avanzada.
Población pediátrica
No se ha evaluado el perfil farmacocinético en la población pediátrica.
05.3 Datos preclínicos sobre seguridad -
Dado que la actividad biológica de denosumab en animales es específica de primates no humanos, se utilizaron evaluaciones de ratones genéticamente modificados (knockout) o el uso de otros inhibidores biológicos de la vía para evaluar las propiedades farmacodinámicas de denosumab en modelos de roedores. RANK / RANKL , como OPG-Fc y RANK-Fc.
En modelos de ratón de metástasis ósea de cáncer de mama humano, receptor de estrógeno positivo y negativo, cáncer de próstata y cáncer de pulmón de células no pequeñas, OPG-Fc redujo las lesiones osteolíticas, osteoblásticas y osteolíticas / osteoblásticas, retrasó la formación de metástasis óseas de novo y reducción del crecimiento tumoral del sistema esquelético. En estos modelos, cuando OPG-Fc se combinó con terapia hormonal (tamoxifeno) o quimioterapia (docetaxel), se encontró una "inhibición adicional del crecimiento tumoral del sistema esquelético. en cáncer de mama y próstata o cáncer de pulmón, respectivamente. En un modelo de ratón de inducción de cáncer de mama, RANK-Fc redujo la proliferación inducida por hormonas en el epitelio mamario y retrasó la formación de tumores.
No se han realizado pruebas estándar para investigar la potencial genotoxicidad de denosumab, ya que estas pruebas no son relevantes para esta molécula. Sin embargo, dadas sus características, es poco probable que denosumab tenga potencial genotóxico.
El potencial carcinogénico de denosumab no se ha evaluado en estudios a largo plazo con animales.
En estudios de toxicidad de dosis única y repetida realizados en monos cynomolgus, las dosis de denosumab que resultaron en una "exposición sistémica de 2.7 a 15 veces la dosis humana recomendada no tuvieron impacto en la fisiología cardiovascular, fertilidad masculina o femenina, o producto de toxicidad de órganos específicos".
En un estudio en monos cynomolgus de dosis múltiples de denosumab durante el período equivalente al primer trimestre del embarazo, las dosis de denosumab que resultaron en una exposición sistémica 9 veces superior a la dosis humana recomendada no indujeron toxicidad materna o daño al feto en un período equivalente al primer trimestre, sin embargo, no se examinaron los ganglios linfáticos fetales.
En otro estudio de monos cynomolgus a los que se les administró denosumab durante el embarazo, a una exposición sistémica 12 veces mayor que la dosis humana, hubo un aumento en el mortinato y la mortalidad postnatal; crecimiento anormal del hueso que resultó en una reducción de la resistencia ósea, reducción de la hematopoyesis y mala alineación dental; ausencia de ganglios linfáticos periféricos; y crecimiento neonatal reducido. No se ha establecido un nivel de dosis que pueda ser negativo para los efectos reproductivos. Posteriormente, a los 6 meses después del nacimiento, los cambios óseos mostraron una recuperación y no hubo efecto sobre la erupción dentaria. Sin embargo, los efectos sobre los ganglios linfáticos y la mala alineación dentaria persistieron, y se observó en una mineralización mínima a moderada en múltiples tejidos (tratamiento correlación incierta) No hubo evidencia de daño materno antes del parto. Los efectos adversos maternos ocurrieron con poca frecuencia durante el trabajo de parto. El desarrollo de la glándula mamaria materna fue normal.
En estudios preclínicos de calidad ósea realizados en monos tratados a largo plazo con denosumab, la disminución del recambio óseo estuvo acompañada de una mejor resistencia ósea y una histología normal.
En ratones machos modificados genéticamente para expresar RANKL humano (ratones knock-in) y sometidos a fractura transcortical, el denosumab retrasó la eliminación del cartílago y la remodelación del callo en comparación con el grupo de control, pero la fuerza biomecánica no se vio afectada negativamente.
Se observó ausencia de lactancia debido a la inhibición de la maduración de la glándula mamaria (desarrollo de las estructuras lobulo-alveolares de la glándula mamaria durante el embarazo) en ratones knockout que no expresaban RANK o RANKL, así como formación alterada en ratones recién nacidos RANK / RANKL knockout que exhibieron También se observó pérdida de peso, disminución del crecimiento óseo, placas de crecimiento alteradas y ausencia de erupción dental. En estudios en ratas recién nacidas que recibieron inhibidores de RANKL, también se observaron crecimiento óseo reducido, placas de crecimiento alteradas y erupción dental alterada; estos cambios fueron parcialmente reversibles tras la interrupción del inhibidor de RANKL Los primates adolescentes tratados con dosis de 2,7 y 15 veces superiores de denosumab (dosis de 10 y 50 mg / kg) mostraron anomalías de la ca. líneas de crecimiento. Por lo tanto, el tratamiento con denosumab puede afectar el crecimiento óseo en niños con placas de crecimiento abiertas e inhibir la erupción dental.
06.0 INFORMACIÓN FARMACÉUTICA -
06.1 Excipientes -
Ácido acético glacial *
Hidróxido de sodio (para ajuste de pH) *
Sorbitol (E420)
Agua para preparaciones inyectables
* El tampón de acetato se obtiene mezclando ácido acético e hidróxido de sodio
06.2 Incompatibilidad "-
En ausencia de estudios de compatibilidad, este medicamento no debe mezclarse con otros medicamentos.
06.3 Período de validez "-
3 años.
XGEVA se puede almacenar a temperatura ambiente (hasta 25 ° C) hasta por 30 días en el empaque original. Una vez sacado del refrigerador, XGEVA debe usarse dentro de este período de 30 días.
06.4 Precauciones especiales de conservación
Conservar en nevera (entre 2 ° C y 8 ° C).
No congelar.
Mantenga el vial en el embalaje exterior para proteger el medicamento de la luz.
06.5 Naturaleza del envase primario y contenido del envase.
1,7 ml de solución en un vial de un solo uso (vidrio tipo I) con un tapón (recubierto con fluoropolímero elastomérico) y un precinto (aluminio) con una cápsula flip-off.
Envase de uno, tres o cuatro viales.
Es posible que no se comercialicen todos los tamaños de envases.
06.6 Instrucciones de uso y manipulación -
Antes de la administración, la solución de XGEVA debe inspeccionarse visualmente. La solución puede contener trazas de partículas de proteína translúcidas a blancas.No inyecte la solución si está turbia o descolorida. No agite excesivamente. Para evitar problemas en el lugar de la inyección, deje que el vial alcance la temperatura ambiente (hasta 25 ° C) antes de la inyección e inyéctelo lentamente. Inyecte todo el contenido del vial. Se recomienda una aguja de acero de calibre 27 para la administración de denosumab. No reutilice el vial.
Los medicamentos no utilizados y los desechos derivados de este medicamento deben eliminarse de acuerdo con las regulaciones locales.
07.0 TITULAR DE LA "AUTORIZACIÓN DE COMERCIALIZACIÓN" -
Amgen Europe B.V.
Minervum 7061
NL-4817 ZK Breda
Países Bajos
08.0 NÚMERO DE AUTORIZACIÓN DE COMERCIALIZACIÓN -
EU / 1/11/703/001
EU / 1/11/703/002
EU / 1/11/703/003
041300017
041300029
09.0 FECHA DE LA PRIMERA AUTORIZACIÓN O RENOVACIÓN DE LA AUTORIZACIÓN -
Fecha de la primera autorización: 13 de julio de 2011
Fecha de la última renovación: 4 de abril de 2016
10.0 FECHA DE REVISIÓN DEL TEXTO -
Diciembre de 2016